题文
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:
①X元素原子的价电子排布式为ns1,且原子半径是同族元素最小的。
②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电子排布式中,p轨道上只有1个未成对电子。
③Z元素的电离能(用符号I表示)数据见表(kJ·mol-1)
I1
I2
I3
I4
…
496
4 562
6 912
9 540
…
请回答:
⑴Z2Y中含有的化学键类型为 。
⑵Z2Y2的电子式为 。
⑶X2Y分子的空间构型为 ,其中心原子的杂化方式为 ,XWY属于________(填“极性”或“非极性”)分子。
题型:未知 难度:其他题型
答案
⑴ 离子键 ⑵
解析
X元素原子的价电子排布式为ns1,且原子半径是同族元素最小的,这说明X是氢元素。Y元素是地壳中含量最多的元素,则Y是氧元素;W元素的电负性略小于Y元素,在W原子的电子排布式中,p轨道上只有1个未成对电子,且W的原子序数大于氧元素的,这说明W应该是氯元素。根据Z元素的电离能可知,Z的第二电离能远远大于第一电离能,这说明Z是第IA族元素,所以根据Z的原子序数可知,Z应该是钠元素。
(1)氧化钠中含有离子键。
(2)过氧化钠中含有离子键和非极性键,则电子式是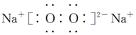
。
(3)水分子中氧原子含有的孤对电子对数=(6-2×1)÷2=2,所以水是V形结构,氧原子是sp3杂化。HClO分子中电荷不能重合,所以是极性分子。
点评:该题是高考中的常见考点,属于中等难度的试题的考查,试题贴近高考,基础性强。侧重对学生灵活运用基础知识解决实际问题的能力,有利于培养学生分析、归纳和总结问题的能力。
考点
据考高分专家说,试题“X、Y、Z、W为按原子序数由小到大排列的.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




