题文
铀
解析

与
的质子数相同,中子数不同,二者互为同位素,化学性质相似,物理性质不同,A不正确;中子数+质子数=质量数,则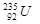
原子核中含有235-92=143个中子,B正确;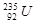
是锕系元素,位于第七周期,属于长周期元素,C不正确;
的的相对原子质量近似是235,所以1mol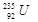
的质量是235g,D不正确,答案选B。
点评:该题是常识性知识等考查,难度不大。主要是考查学生对原子组成以及组成原子的几种微粒之间数量关系的了解掌握情况,意在培养学生分析、概念和总结问题的能力。
考点
据考高分专家说,试题“铀是重要的核工业原料,在自然界中的含量很.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




