题文
利用15N可以测定亚硝酸盐对地下水质的污染情况。
(1)下列说法正确的是___。A.14N与15N为同种核素B.14N的第一电离能小于14CC.15NH3与14NH3均能形成分子间氢键D.CH315NH2与CH3CH214NH2互为同系物(2)15N的价层电子排布图为_______15NH4Cl的晶胞与CsCl相同,则15NH4Cl晶体中15NH4+的配位数为_______;15NH4+中I5N的杂化轨道类型为_______。
(3) 工业上电解法处理亚硝酸盐的模拟工艺如图。
解析
(1) 14N与15N质子数相同、中子数不同,互称为同位素,不是同种核素,A错误;同周期元素从左向右,第一电离能总体趋势增大,但IIA和VA反常,第一电离能:N>C,B错误;N电负性大,NH3分子间存在氢键,C正确;同系物指结构相似,分子组成相差n个CH2,D正确。
(2)N价层电子排布为2s22p3,轨道表示式为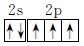
;CsCl中Cs+和Cl-配位数均为8;15NH4+中N价层电子对数=
=4,N杂化类型为sp3。
(3)① 阳极为Fe,电极反应式为Fe-2e-=Fe2+。②若硫酸浓度过大,阴极发生2H++2e-=H2↑,阴极产生氢气。说明氢离子浓度越大,氧化性越强。③若电解时转移0.6mol电子,则由Fe-2e-=Fe2+得阳极生成0.3molFe2+,由阳极区化学反应得消耗NaNO20.1mol,所以生成硫酸钠0.05mol。
考点
据考高分专家说,试题“利用15N可以测定亚硝酸盐对地下水质的污.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




