题文
短周期元素A、B、C、D在元素周期表中的相对位置如图所示,其中B所处的周期序数与族序数相等。填写下列空白。
A
B
C
D
(1)写出C的氧化物的一种用途:
(2)B单质与Fe2O3反应时,每消耗13.5g B时放热213kJ,该反应的热化学方程式是
(3)为防止A元素的氧化物AO2污染空气,科学家寻求合适的化合物G和催化剂,以实现反应:
AO2+X催化剂A2 +H2O+n Z(未配平,n可以为0)。上述反应式中的X不可能是 (填标号)。
a.NH3 b.CO c.CH3CH2OH d.H2O2
(4)A元素的最简单氢化物甲、D元素的最高价氧化物对应的水化物乙都是很重要的基础化工原料。
①一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是 (选填序号)。
选项
a
b
c
d
x
温度
温度
加入H2的物质的量
加入甲的物质的量
y
甲的物质的量
平衡常数K
甲的转化率
生成物物质的量总和
②25℃时,往a mol·L-1的甲的水溶液中滴加0.01 mol·L-1乙溶液,当两种溶液等体积混合时,溶液呈中性(设温度不变)。滴加过程中溶液的导电能力 (填“增强”、“减弱”或“不变”);
所得混合溶液中A、D两种元素的物质的量的关系为:A 2D(填“大于”、“等于”或“小于”);甲中溶质的电离平衡常数Kb= (用含a的代数式表示)。
题型:未知 难度:其他题型
答案
(14分,7空,每空2分)(1)制备单晶硅、玻璃、光导纤维、建筑材料等(合理答案即可给分)
(2)2Al(s)+Fe2O3(s)=2Fe(s)+Al2O3(s) △H=-852kJ·mol-1
(3)b (4) ①a、c ; ②增强 ; 大于;
解析
根据元素在周期表中的相对位置可知,B是第三周期元素。又因为B所处的周期序数与族序数相等,所以B是铝元素,则A是N,C是Si,D是S。
(1)硅的氧化物二氧化硅的主要用途是制备单晶硅、玻璃、光导纤维、建筑材料等。
(2)B单质与Fe2O3反应的化学方程式是2Al+Fe2O3
2Fe+Al2O3,由于每消耗13.5g B时放热213kJ,则消耗2mol铝放出的热量是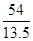
×213kJ=852kJ,因此该反应的热化学方程式是2Al(s)+Fe2O3(s)=2Fe(s)+Al2O3(s) △H=-852kJ/mol。
(3)根据方程式可知,NO2中氮元素的化合价从+4价降低到0价,得到电子,发生还原反应。则X一定失去电子,做还原剂。又因为反应中还有水生成,这说明X中一定含有氢元素,所以X不可能是CO,答案选b。
(4)①氨气分解的方程式是2NH3
N2+3H2,该反应是体积增大的吸热的可逆反应。升高温度平衡向正反应方向移动,氨气的物质的量减少,a正确;升高温度平衡向正反应方向移动,平衡常数增大,b不正确;增加氢气的物质的量,平衡向逆反应方向移动,氨气的转化率降低,c正确;增加氨气的物质的量,平衡向正反应方向移动,生成物的物质的量增加,d不正确,答案选ac。
②一水合氨是弱电解质,加入硫酸生成强电解质硫酸铵,因此溶液的导电能力增强;如果二者恰好反应生成硫酸铵,则溶液中NH4+水解,溶液显酸性。如果溶液显中性,则说明氨水过量,所以所得混合溶液中A、D两种元素的物质的量的关系为:A大于2D;根据电荷守恒可知c(H+)+c(NH4+)=c(OH-)+2c(SO42-),溶液显中性,则c(H+)=c(OH-),所以c(NH4+)=2c(SO42-)=2×
×0.01mol/L=0.01mol/L。根据氮元素守恒可知,溶液中c(NH3·H2O)=
×amol/L-0.01mol/L,所以根据电离平衡NH3·H2O
NH4++OH-可知,该温度下氨水的电离平衡常数Kb=
=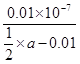
=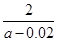
×10-9。
考点
据考高分专家说,试题“短周期元素A、B、C、D在元素周期表中的.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




