题文
有X、Y、Z、W四种含14个电子的粒子,其结构特点如下:
粒子代码
X
Y
Z
W
原子核数
单核
不同元素构成的两核
同元素构成的两核
同元素构成的两核
粒子的电荷数
0
0
两个负电荷
0
(1)A原子核外比X原子多3个电子,A的原子结构示意图是 。含lmolX的氧化物晶体中含有共价键数目为 。
(2)Z与钙离子组成的化合物的电子式为 。
(3)14gY完全燃烧放出的热量是141.5kJ,写出Y燃烧的热化学方程式 。
(4)组成W的元素最高价氧化物对应的水化物甲有下图所示转化关系(丁为金属单质,反应条件和其他物质已略)
解析
根据题意可知这四种物质分别是:X为Si,Y为CO,Z为C22_,Z为N2.(1)X为14号元素Si,则A 为17元素氯。其原子结构示意图略。二氧化硅为原子晶体,每个Si原子与4个O原子通过共价键结合,故含lmolSi的氧化物晶体中含有共价键数目为4NA或2.408×1024.
(2)由于Z为C22_,Z与钙离子组成的化合物的电子式
(3)Y为CO,其摩尔质量为28g/mol.n(CO)="0.5" mol其热化学方程式为:2CO(g)+O2(g)=2CO2(g);△H=-566kJ/mol.其他合理答案也可得分。
(4)①由题意知甲为HNO3,能与硝酸反应,且加入的量多少不同,产物不同的金属只有Fe,其在元素周期表中位于第四周期第Ⅷ族,②在高温下铁与水反应的化学方程式是: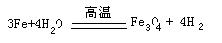
③NH3、H2O都是极性分子,NH3、H2O之间除了分子间的作用力外,还存在存在氢键,增加了相互作用。根据相似相溶原理,氨气易溶解于水。氨气与空气组成的燃料电池,氨气为负极,空气为正极。其负极的电极反应式为2NH3-6e-+6OH-=N2+6H2O。
考点
据考高分专家说,试题“有X、Y、Z、W四种含14个电子的粒子,.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




