题文
(12分)U、V、X、Y、Z五种短周期元素,原子序数依次增大。U、V两元素最高正价与最低负价之和均为0;Y与U同主族;X、Z分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(用实际元素符号表示)________________;
(2)由这五种元素中的几种组成的化合物A、B、C、D有如下转化关系:
解析
由“X、Z分别是地壳中含量最高的非金属元素和金属元素”知,X为氧元素,Z为铝元素,由“U、V两元素最高正价与最低负价之和均为0”,知两元素可能位于第ⅠA族或第ⅣA族,结合“U、V、X、Y、Z五种短周期元素,原子序数依次增大”和“Y与U同主族”知,U为氢元素,V为碳元素,Y为钠元素。(l)结合原子半径比较原则知,五种元素原子半径由大到小的顺序是Na>Al>C>O>H;(2)由这五种元素中的几种组成的化合物A、B、C、D有如下转化关系: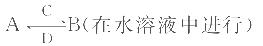
其中C是溶于水显酸性的气体;D是淡黄色固体。则C为CO2,D为Na2O2,二者反应的化学方程式为:2Na2O2 + 2CO2 = 2Na2CO3 + O2;①B为两性不溶物,结合转化关系可知,A为四羟基合铝酸钠、B为氢氧化铝,四羟基合铝酸根与二氧化碳反应生成氢氧化铝,反应离子方程式为:[Al(OH)4]-+CO2 = Al(OH)3↓+ HCO3-;②B由四种元素组成,B溶液显碱性,结合转化关系可知,A为碳酸钠、B为碳酸氢钠,碳酸氢钠在化学键类型为离子键、共价键;碳酸钠属于盐。
考点
据考高分专家说,试题“(12分)U、V、X、Y、Z五种短周期元.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




