题文
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题: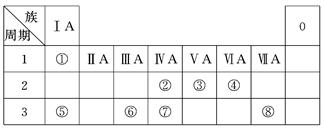
(1)④、⑤、⑥的原子半径由大到小的顺序是____________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:______________。
(4)写出由②、③、④中的元素形成的等电子体分子 。(任写一组)
(5)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(6)由表中①、③、④三种元素形成盐的水溶液呈酸性,用离子方程式表示其原因: ;由表中①、②、③、④四种元素形成的一种盐的水溶液呈中性,该盐的化学式是 。
题型:未知 难度:其他题型
答案
(1)Na>Al>O(1分)
(2)HNO3>H2CO3>H2SiO3(1分)
(3)
或
(2分)
(4)N2 、CO(或N2O、CO2)(2分)
(5)ab(2分,漏选得1分,错选,多选均不得分)
(6)NH4++H2O
NH3·H2O + H+ (2分) CH3COONH4(2分)
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
依据元素①~⑧在表中的位置可知,它们分别是H、C、N、O、Na、Al、Si、Cl。
(1)同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,所以④、⑤、⑥的原子半径由大到小的顺序是Na>Al>O。
(2)非金属性越强,最高价氧化物对应水化物的酸性越强。同周期自左向右非金属性逐渐增强,同主族自上而下非金属性逐渐减弱,则②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3。
(3)H、O、Na、Cl中的某些元素可形成既含离子键又含极性共价键的化合物可以是氢氧化钠或次氯酸钠等,其电子式为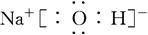
或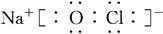
。
(4)原子数和价电子数分别都相等的是等电子体,则由C、N、O中的元素形成的等电子体分子是N2 、CO(或N2O、CO2)。
(5)两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,则该化合物是双氧水。其中可以起到催化剂作用的是MnO2、FeCl3,答案选ab。
(6)H、N、O三种元素形成盐的水溶液呈酸性,则该化合物是硝酸铵。硝酸铵溶于水电离出的NH4+水解溶液显酸性,离子方程式为NH4++H2O
NH3·H2O + H+。H、C、N、O四种元素形成的一种盐的水溶液呈中性,该盐的化学式是醋酸铵。由于NH4+与CH3COO-的水解程度相同,因此溶液显中性。
考点
据考高分专家说,试题“下表为元素周期表的一部分,请参照元素①~.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




