题文
自然界中的水要经过消毒杀菌才可成为生活饮用水。ClO2是一种高效安全灭菌消毒剂,
其中Cl化合价为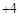
价。
(1)氯原子最外层有 种能量不同的电子,某化合物中O的化合价与ClO2中O的化合价恰好相反,写出该化合物的分子式 。
(2)下列可用作比较S和C非金属性强弱依据的是
A.CS2中各元素的化合价 B.气态氢化物的稳定性
C.元素在周期表中的位置 D.最高价含氧酸的酸性
(3)以下性质的比较正确的是
A.键长:HF>HCl B.稳定性:HF>HCl
C.酸性:HF>HCl D.沸点:HF>HCl
O3也是一种很好的消毒剂,具有高效、洁净、方便、经济等优点。O3可溶于水,在水中易分解,产生的[O]为游离氧原子,有很强的杀菌消毒能力。常温常压下发生反应如下:
反应① O3
O2 +[O]-Q 平衡常数为K1 ;
反应② [O]+O3
2O2+Q 平衡常数为K2 ;
总反应:2O3
3O2+Q 平衡常数为K。
(4)一定条件下,O3的浓度减少一半所需的时间(t)如下表所示。
已知:O3的起始浓度为0.0216 mol/L。
pH
t / min
T / ℃
3.0
4.0
5.0
6.0
20
301
231
169
58
30
158
108
48
15
50
31
26
15
7
在30°C、pH=4.0条件下,O3的分解速率为_______________ mol/ (L·min)。
(5)根据表中数据,推测O3在下列条件下分解速率由小到大的顺序为________。(填字母代号)
A.40°C、pH=3.0 B.10°C、pH=4.0 C.30°C、pH=7.0
(6)下列叙述正确的是
A.降低温度,K增大 B.K=K1+K2
C.适当升温,可提高消毒效率 D.压强增大,K2减小
题型:未知 难度:其他题型
答案
(1)2 (1分) OF2 (1分)
(2)AD (2分)
(3)BD (2分)
(4)1×10—4 (2分)
(5)B(6)AC (2分)
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
(1)氯原子最外层电子排布式为3S2SP5,3S,3P两种轨道,故有2种能量不同的电子,某化合物中O的化合价与ClO2中O的化合价恰好相反,应该为+2价,该化合物的分子式 OF2 。
(2)A中CS2中各元素的化合价为负的说明得电子能力强,非金属性强,正确。B.气态氢化物的稳定性越强其对应元素的非金属性越强,正确。C.两中元素在周期表中的位置无法进行判断,错误。D.最高价含氧酸的酸性硫酸强于碳酸,正确。选ABD。
(3)A.由于F原子半径小于氯,故键长HF
(4)根据表中数据在30°C、pH=4.0条件下,O3的分解速率为0.0216/(2*108)=1×10—4mol/ (L·min)。
(5)根据表中数据,O3在下列条件下分解速率由小到大的顺序为B(6)正反应是放热反应,A中降低温度平衡正向移动,K增大,正确。B中应该是K=K1*K2,错误。C.适当升温,平衡右移,使溴氧的量较多,可延长消毒,正确。D中K2不变,只与温度有关,错误。
考点
据考高分专家说,试题“自然界中的水要经过消毒杀菌才可成为生活饮.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




