题文
短周期元素X、Y、Z、L、M、Q的原子半径和主要化合价见下表
元素代号
X
Y
Z
L
M
Q
原子半径/nm
0.160
0.143
0.102
0.099
0.077
0.074
主要化合价
+2
+3
+6、-2
+7、-1
+4、-4
-2
就以上6种元素,用化学用语回答下列问题
(1)同主族的元素是 ,
(2)写出同周期元素间形成的常温下是有毒气体化合物的分子式为 ,
(3)写出不同周期的元素间形成的常温下为液体且难溶于水的任意一种化合物的电子式 。
(4)等质量的X、Y的单质与足量盐酸反应,生成H2的物质的量之比为
(5)写出由表中元素形成的物质间发生常见的置换反应的化学方程式
题型:未知 难度:其他题型
答案
(1)S O (不分先后)(2分)
(2) CO (2分)
(3)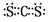
或 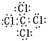
(2分)
(4)3:4 (2分)
(5)2Mg+ CO2
2MgO + C (2分)
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
根据元素原子的半径和主要化合价可判断,X是Mg,Y是Al,Z是S,L是Cl,M是C,Q是O。
(1)同主族的元素是S,O ;
(2)同周期元素间形成的常温下是有毒气体化合物的分子式为CO;
(3)不同周期的元素间形成的常温下为液体且难溶于水的化合物要么是CCl4,要么是CS2,电子式
或 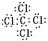
;
(4)等质量的Mg、Al的单质与足量盐酸反应,
Mg ~ H2 2Al ~ 3H2
24g 1mol 2×27g 3mol
1g xmol 1g ymol
生成H2的物质的量之比为x:y=3:4;
(5)表中元素形成的物质间发生常见的置换反应的化学方程式 2Mg+ CO2
2MgO + C,2H2S+O2
2H2O+2S,H2S+Cl2=2HCl+S↓。
考点
据考高分专家说,试题“短周期元素X、Y、Z、L、M、Q的原子半.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




