题文
现有部分短周期元素的性质或原子结构如下表:
元素编号
元素的性质或原子结构
X
最外层电子数是次外层电子数的3倍
Y
常温下单质是双原子分子,其氢化物的水溶液显碱性
Z
第三周期元素的简单离子中半径最小
(1)元素X的一种单质在生活中常用作饮水机的消毒剂,该单质的化学式是 ,元素Z的离子结构示意图为 。
(2)元素Y与氢元素形成一种离子YH4+,请写出检验溶液中存在该离子的实验操作、现象和结论 。
(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式: 。
(4)元素X与元素Y相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 。
a.Y的氢化物可在纯X2中燃烧生成X的氢化物和Y2
b.X的单质比Y的单质更容易与H2化合
c.X与Y形成的化合物中Y元素呈正价态
题型:未知 难度:其他题型
答案
(1)O3;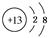
(2)取少量溶液(或待测液)于试管中,滴加适量浓NaOH溶液后加热,将湿润的红色石蕊试纸黏在玻璃棒上靠近试管口,若试纸变蓝,说明溶液中存在该离子,反之,则不存在该离子 (3)Al(OH)3+OH-=AlO2-+2H2O (4)O;abc
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
根据X、Y、Z三种元素的性质或原子结构可以判断X为氧元素,Y为氮元素,Z为铝元素。(1)O3在生活中常用作饮水机的消毒剂,元素Z的离子为Al3+。(2)检验溶液中NH4+的实验操作为:取少量溶液(或待测液)于试管中,滴加适量浓NaOH溶液后加热,将湿润的红色石蕊试纸黏在玻璃棒上靠近试管口,若试纸变蓝,说明溶液中存在该离子,反之,则不存在该离子。(3)Z元素最高价氧化物对应的水化物为Al(OH)3。(4)X、Y的单质与H2化合的难易程度,氢化物的稳定性,以及X与Y形成的化合物中,Y元素呈正价态均说明N元素与O元素相比,氧元素的非金属性较强。
考点
据考高分专家说,试题“现有部分短周期元素的性质或原子结构如下表.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




