题文
A是有机羧酸盐,B、C、D是常见化合物; A、B、C、D焰色反应呈黄色,水溶液均呈碱性,其中B的碱性最强。X、Y是最常见的氧化物且与人体、生命息息相关,它们的晶体类型相同。A与B等物质的量反应生成D和一种气体单质;C受热分解得到Y、D和X;B与C反应生成D和X。E由两种元素组成,式量为83,将E投入X中得到B和气体Z,Z在标准状况下的密度为0.76g·L-1。
(1)A的化学式是 。Y的电子式是 。
(2)X的沸点比同主族同类型物质要高,原因是 。
(3)写出E与足量盐酸反应的化学方程式
(4)写出在D的饱和溶液中不断通Y析出C的离子方程式 。
(5)A的一个重要应用是根据2A →P +H2↑得到P,P溶液中的阴离子通常用CaCl2使之沉淀,当它完全沉淀时,溶液中Ca2+的物质的量浓度至少为 。
(沉淀Ksp=2.3×10-9,当溶液中离子浓度≤10-5mol·L-1,即可认为完全沉淀)
(6)实验室常用P与足量HCl反应所得的有机物在浓硫酸条件下共热分解制某还原性气体,设计实验证明分解产物中还原性气体的存在 。
题型:未知 难度:其他题型
答案
(1)HCOONa(2分) 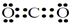
(2分)
(2)水分子间存在氢键(2分)
(3)Na3N+4HCl=3NaCl+NH4Cl(2分)
(4)2Na++CO32-+H2O+CO2==2NaHCO3↓(2分)
(5)2.3×10-4mol·L-1(2分)
(6)将所得气体先通过足量NaOH溶液,再通过澄清石灰水,无现象,点燃剩余气体,将事先用澄清石灰水润湿过的烧杯倒置在火焰上方,烧杯内壁变浑浊,说明有还原性气体CO的存在。(3分)(其它合理答案也给分)
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
① 已知A是有机羧酸盐,B、C、D是常见化合物; A、B、C、D焰色反应呈黄色,水溶液均呈碱性。则可推知化合物A、B、C、D均为含有Na元素的碱或强碱弱酸盐,B的碱性最强,则B为NaOH。② X、Y是最常见的氧化物且与人体、生命息息相关,它们的晶体类型相同,则X、Y应为H2O和CO2。③ 由C受热分解得到Y、D和X;B与C反应生成D和X,可推知C为NaHCO3,D为Na2CO3;即2 NaHCO3
Na2CO3 +CO2↑+H2O; NaHCO3 +NaOH =Na2CO3 +H2O; 由此可确定X为H2O,Y为CO2。④ 由有机羧酸盐A与NaOH等物质的量反应生成Na2CO3和一种气体单质,可联想到由无水醋酸钠与NaOH加热反应制取甲烷的脱羧反应: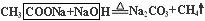
,由此迁移可知,A为甲酸钠(HCOONa),与等物质的量NaOH进行脱羧反应生成Na2CO3和氢气: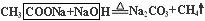
。⑤ E由两种元素组成,式量为83,将E投入H2O中得到NaOH和气体Z,Z在标准状况下的密度为0.76g·L-1。由计算可知气体Z的相对分子质量是17,则Z为NH3,由该反应:E + H2O → NaOH + NH3↑,可推知E由Na和N两种元素组成,再根据元素化合价可确定E是Na3N。
由此可解答:
(1)A的化学式是 HCOONa ;Y的电子式是 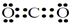
(2)X的沸点比同主族同类型物质要高的原因是:水分子间存在氢键,从而使分子间作用力增加,因此有较高的沸点。
(3)E与足量盐酸反应的化学方程式:Na3N + 4HCl =" 3NaOH" + NH4Cl 。
(4)D的饱和溶液中不断通入通Y析出C的离子方程式为:
2Na++CO32-+H2O+CO2 = 2NaHCO3↓
(5)根据2A →P +H2↑得到P,可知,2HCOONa →Na2C2O4 + H2↑,P为Na2C2O4,C2O42- + Ca2+ = CaC2O4↓,依据Ksp(CaC2O4) = c(Ca2+)•c(C2O42-) = 2.3×10-9,可计算出当CaC2O4完全沉淀时,溶液中Ca2+的物质的量浓度至少为:c(Ca2+) =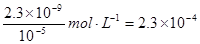
mol•L-1
(6)实验室Na2C2O4与足量HCl反应可得到H2C2O4 ,H2C2O4在浓硫酸条件下共热分解生成CO、CO2、H2O ( 即 H2C2O4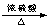
CO↑ + CO2↑+ H2O )。设计证明分解产物中存在还原性气体CO的实验为:将所得气体先通过足量NaOH溶液(或通过盛有固体NaOH的干燥管),再通过澄清石灰水,若无现象,点燃剩余气体,将事先用澄清石灰水润湿过的烧杯倒置在火焰上方,烧杯内壁变浑浊,说明有还原性气体CO的存在。
考点
据考高分专家说,试题“A是有机羧酸盐,B、C、D是常见化合物;.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




