题文
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
a
b
c
d
e
f
g
试回答下列问题(凡涉及的物质均用化学式表示):
(1)a的氢化物的分子构型为 ,中心原子的杂化形式为 ;d的最高价氧化物的分子构型为 ,中心原子的杂化形式为 ,该分子是 (填“极性”或“非极性”)分子。
(2)b、d、e三种元素的氢化物中的沸点最高的是 ,原因是: 。
(3)将g的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子,写出该配合离子的结构简式(必须将配位键表示出来) 。
(4)f(NH3)5BrSO4可形成两种配合物 ,已知f 3+ 的配位数是6,为确定f的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,第二种配合物的化学式为 ,该配合物的配体是 、 ;
(5)c单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。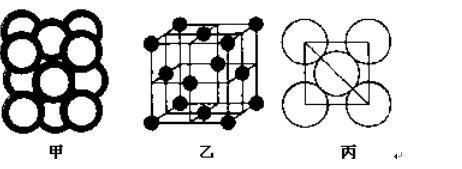
c单质晶体中原子的配位数为 。若已知c的原子半径为r,NA代表阿伏加德罗常数,c的相对原子质量为M。该晶体的密度为 (用字母表示)。
题型:未知 难度:其他题型
答案
1) 三角锥 sp3 平面三角形 sp2 非极性分子
(2)HF ,HF中有氢键
(3)
(4)[Co(NH3)5SO4]Br, NH3、SO42-
(5) 12、 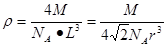
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
根据元素在周期表中的位置可确定a是N;b是F;c是Al;d是S;e是Cl;f是Co;g是Cu。(1)NH3分子构型为三角锥型;中心原子N的杂化形式为sp3杂化;SO3分子构型为平面三角形;中心原子S的杂化形式为sp2;由于各个化学键的排列是对称的,所以该分子是非极性分子。(2)在HF、H2S、HCl三种物质中由于在HF的分子之间存在氢键,增加了分子之间的相互作用力,所以HF的沸点最高。(3)在溶液中Cu2+是以四水和铜离子的形式存在的,其结构简式是
。(4)Co(NH3)5BrSO4。Co3+ 的配位数是6可形成两种配合物为确定f的配合物的结构,在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,证明SO42-不是配位体;在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,证明在化合物中SO42-是配位体。则第二种配合物的化学式[Co(NH3)5SO4]Br;该配合物的配体是NH3及SO42-。(5)Al单质晶体中原子的堆积方式为立方面心堆积。则Al单质晶体中原子的配位数为(3×8)÷2=12;在每个晶胞中含有的Al原子的个数为8×1/8+6×1/2=4.由于的原子半径为r,所以晶胞的边长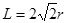
。则该晶体的密度为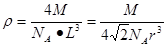
。
考点
据考高分专家说,试题“下表是元素周期表的一部分。表中所列的字母.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




