题文
(12分)根据下列某些短周期元素中元素性质回答问题。
①
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
原子半径/10 -10m
0.37
1.86
0.74
1.43
0.77
1.10
0.99
1.52
0.75
0.71
最高价态
+1
+1
+3
+4
+5
+7
+1
+5
最低价态
-1
-2
-4
-3
-1
-3
-1
(1)元素③、⑥和⑨的氢化物中沸点由高到低的顺序是__________ (填化学式)。
(2)元素①和⑨形成阳离子 ,其结构式为__________________。
(3)某元素R的原子半径为1.02×10 -10m ,它与钠形成Na2R2,其电子式是_________(R用元素符号表示)。
(4)元素②和⑦形成晶体的部分结构可用下图中的_________来表示(填序号)。
(5)①、③、⑨可以形成原子个数之比为4:3:2的中学常见无机化合物,该化合的水溶液显酸性的原因是_________________(用离子方程式表示),其水溶液中离子浓度由大到小的顺序是___________________。
题型:未知 难度:其他题型
答案
(1)H2O、NH3、PH3; (2) 
(3)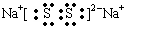
(4) A
(5) NH4+ + H2O 
NH3.H2O + H+ ; C(NO3--) > C(NH4+) > C( H+) > C(O H--)
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
根据搞个的数据经方向可得:①是H;②是Na;③是O;④是Al;⑤是C;⑥是P;⑦是Cl;⑧是Na;⑨是N;⑩是F。(1)元素③、⑥和⑨的氢化物分别是H2O、PH3、 NH3;元素的非金属性O>N>P,这几种物质都是分子晶体。分子间通过分子间作用力结合。由于在H2O、NH3的分子之间除了存在分子间作用力外还存在氢键,增加了分子之间的相互作用,所以沸点最低的是PH3。由于O元素的非金属性比N强,所以H2O的氢键也强于NH3。因此三种物质中沸点由高到低的顺序是H2O> NH3>PH3。(2)元素H和N可形成阳离子NH4+ ,其结构式为
;(3)某元素R的原子半径为1.02×10 -10m,介于P与Cl原子半径之间,所以该元素是S。所以它与钠形成Na2S2的电子式是
;(4)元素Na和Cl形成NaCl晶体是离子晶体。阳离子与阴离子的配位数但是6个。其结构可用A表示。(5)H、O、N可以形成原子个数之比为4:3:2的中学常见无机化合物是NH4NO3,该物质是强酸弱碱盐,铵根离子水解消耗水电离产生的OH-,使溶液中的H+浓度增大,因此溶液显酸性。水解的离子方程式为NH4+ + H2O 
NH3.H2O + H+ ; NH4NO3= NH4+ + NO3--。铵根离子水解消耗,所以C(NO3--) > C(NH4+);由于水解消耗了OH-,最终溶液中的H+浓度大于OH-的浓度。即C( H+) > C(O H--);盐的电离远大于弱电解质水的电离。因此C(NH4+) > C( H+)。综上所述,在溶液中离子浓度的关系是C(NO3--) > C(NH4+) > C( H+) > C(O H--)。
考点
据考高分专家说,试题“ (12分)根据下列某些短周期元素中元素.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




