题文
(10分).
Ⅰ. 下表列出了A~R 9种元素在周期表中的位置(填元素符号):
主族
周期
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
0
2
E
F
3
A
C
D
G
R
4
B
H
(1) 这9种元素中化学性质最不活泼的是__________,
(2) A、B、C三种元素按原子半径由大到小的顺序排列为
(3) F元素氢化物的化学式是
(4) G元素跟B元素形成化合物的电子式是
(5) G元素和H元素两者核电荷数之差是
Ⅱ 根据原子结构的有关知识和元素周期律。思考并回答有关114号元素的几个问题。
原子核外有_____个电子层,最外层电子数可能是__________
周期表中位于__________周期,________族
(3) 属于_________元素(填金属或非金属)
题型:未知 难度:其他题型
答案
Ⅰ(1)Ar (2)K>Na>Mg (3)H2O (4) 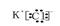
(5)18
Ⅱ(1) 7,4 (2) 第七周期、ⅣA (3)金属
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
Ⅰ、从表中可以判断出A、B、C、D、E、F、G、H、R分别为:Na、K 、Mg、Al、C、O、Cl、Br、Ar。 (1)最不活泼的为0族元素,Ar ;(2) A、B原子核外电子层数不同,电子层数越多,原子半径越大,即K>Na,A于C原子核外电子层数相同,核内质子数越多,原子半径越小,即Na>Mg;(5) G元素和H元素两者核电荷数之差于第四周期中包含的元素种类相同即18。
Ⅱ、根据周期表的结构可以推测114号元素属于第七周期,ⅣA族,周期数等于核外电子层数,主族序数等于最外层电子数,即原子核外有7个电子层,最外层电子数可能是4;属于金属元素。
考点
据考高分专家说,试题“(10分).Ⅰ. 下表列出了A~R 9种.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




