题文
下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
(1)已知由①、③、④三种元素组成的某种常见化合物的水溶液呈酸性,则符合该条件的化合物的化学式可能为 (至少写两种)。
(2)由表中①、④两种元素按原子个数比为1∶1构成的化合物的稀溶液易被催化分解,通常使用的催化剂为 (填序号)。
a. MnO2 b. FeCl3 c、Na2SO3 d、KMnO4
(3)下图中A~F是由部分上表中元素组成的单质或化合物,其中A、B、C为单质,转化关系如下: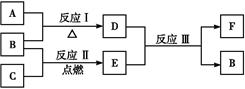
Ⅰ.若B为黄色固体,A为原子半径最小的原子组成的单质。
①F的电子式为 。
②实验测得起始参加反应的B和最后生成的B质量相等,则起始参加反应的A和C的物质的量之比是 。
Ⅱ.若D为淡黄色固体,焰色反应为黄色,组成C的元素的原子最外层电子数是内层电子数的2倍。
①下列关于D的说法正确的是 (填字母)。
a.能与水发生化合反应 b.既有氧化性,又有还原性
c.既含离子键,又含非极性共价键 d.是一种碱性氧化物
②用惰性电极将F的饱和溶液进行电解,则阳极反应式是 。
题型:未知 难度:其他题型
答案
(1)HNO3、NH4NO3(合理即可)
(2)ab (3)Ⅰ.①
②2∶1 Ⅱ.①bc ②4OH--4e-
2H2O+O2↑
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
根据元素在周期表中的相对位置可知,①为H,②为C,③为N,④为O,⑤为Na,⑥为Al,⑦为Si,⑧为S,⑨为Cl。(1)由H、N、O三种元素组成的某种常见化合物的水溶液呈酸性,则符合该条件的化合物的化学式可能为HNO3、NH4NO3。(2)由H、O两种元素按原子个数比为1∶1构成的化合物H2O2的稀溶液易被催化分解,通常使用的催化剂为MnO2或FeCl3,选ab。(3)Ⅰ.若B为黄色固体, A为原子半径最小的原子组成的单质,结合题给转化关系知,A为氢气,B为S, C为氧气,D为硫化氢,E为二氧化硫, F为水。①F为水,电子式为
;②发生的反应H2+S
H2S,S+O2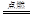
SO2,SO2+2H2S=3S+2H2O,由反应方程式知,参加反应的硫和最后生成的硫质量相等,则起始参加反应的氢气和氧气的物质的量之比是2∶1;Ⅱ.若D为淡黄色固体,焰色反应为黄色,则D为过氧化钠;组成C的元素的原子最外层电子数是内层电子数的2倍,则C为碳;结合转化关系可知,A为Na、B为氧气、E为二氧化碳、F为碳酸钠,①a.过氧化钠与水反应生成氢氧化钠与氧气,不属于化合反应,错误;b.过氧化钠中氧元素为-1价,处于中间价态,过氧化钠既有氧化性,又有还原性,正确;c.过氧化钠属于离子化合物,过氧根离子中氧原子之间形成非极性键,既含离子键,又含非极性共价键,正确;d.过氧化钠不是碱性氧化物,错误;选bc;②用惰性电极将碳酸钠的饱和溶液进行电解,实质为电解水,阳极氢氧根离子放电,电极反应式是4OH--4e-=2H2O+O2↑。
考点
据考高分专家说,试题“ 下表为元素周期表的一部分,请参照元素①.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




