题文
(14分)(1) 把除去氧化膜的铁丝投入到盛有稀硫酸的试管中,产生氢气 的速率变化情况如图所示图中t1~t2速率变化的主要原因是 ,t2~t3速率变化的主要原因是 。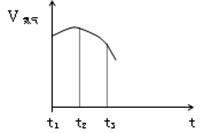
(2)甲、乙、丙、丁是四种短周期元素,乙原子中K层与M层电子数相等;甲原子的核 外电子数比乙原子核外电子数少1;丙原子的最外层电子数是次外层电子数的2倍;丁原子核电荷数比丙原子核电荷数多2。请回答:
①甲的单质与水反应的离子方程式为 ;②乙元素在周期表中的位置为 ;③丙元素的最高价氧化物的电子式为 ;④甲与丁两种元素可组成的具有强氧化性的物质是 。(填化学式)
(3)某元素R,它的最高价含氧酸的阴离子是RO4ˉ,则其气态氢化物的化学式是 。
题型:未知 难度:其他题型
答案
(1) 铁与硫酸的反应是放热反应,溶液温度升高,反应速率加快;(放热反应1分;温度升高1分)
硫酸酸浓度减小,反应速率减慢。(浓度减小给2分)
(2)2Na+2H2O==2Na++2OH-+H2↑ ;第三周期第ⅡA族 ;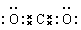
;Na2O2
(3)HR
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
(1)把除去氧化膜的铁丝投入到盛有稀硫酸的试管中,产生氢气的速率变化情况如右图所示图中t1~t2速率变化的主要原因是铁与硫酸的反应是放热反应,放出热量是溶液的温度升高,升高温度,化学反应速率加快;随着反应的进行,溶液变稀,这时影响化学反应速率的主要因素是物质的浓度。由于t2~t3时主要是物质浓度的影响,所以化学反应速率减慢。(2)根据题意可知甲是Na;乙是Mg;丙是C;丁是O。①甲的单质与水反应的离子方程式为2Na+2H2O==2Na++2OH-+H2↑;②乙元素在周期表中的位置为第三周期第ⅡA族;③丙元素的最高价氧化物的电子式为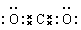
;④甲与丁两种元素可组成的具有强氧化性的物质的化学式是Na2O2。(3)某元素R,它的最高价含氧酸的阴离子是RO4ˉ,则其最高化合价是+7价,由于同一种元素的最高化合价与最低化合价绝对值的和为8,在其氢化物中为最低化合价,所以为-1价,则其气态氢化物的化学式是HR。
考点
据考高分专家说,试题“(14分)(1) 把除去氧化膜的铁丝投入.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




