题文
(9分)下表是元素周期表的一部分:
针对表中的①~⑩号元素,用元素符号或化学式填空:
(1)在这些元素中,最易失电子的元素是 ,非金属性最强的元素是 。
(2)化学性质最不活泼的元素是 ,其原子结构示意图为 。
(3)元素的最高价氧化物对应的水化物中呈两性的氢氧化物与氢氧化钠溶液反应的离子方程式是 。
(4)在②⑤⑦⑨四种元素中,原子半径由大到小的顺序是 。
(5)元素⑥、⑩的最高价氧化物对应的水化物中,酸性较强的是 。
题型:未知 难度:其他题型
答案
(1)K(1分) F(1分) (2)Ar(1分) 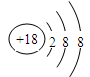
(1分)
(3)Al(OH)3+OH-=[Al(OH)4]-(2分) (4)K>Si>Cl>F (2分) (5)H2SO4(1分)
点击查看构成物质的粒子—分子、原子、离子知识点讲解,巩固学习
解析
根据元素在周期表中的相对位置可知①~⑩号元素分别是N、F、Mg、Al、Si、S、Cl、Ar、K、Se。则
(1)同周期自左向右金属性逐渐减弱,非金属性逐渐增强,同主族自上而下金属性逐渐增强,非金属性逐渐减弱,则在这些元素中,最易失电子的元素是K,非金属性最强的元素是F。
(2)化学性质最不活泼的元素是稀有气体元素Ar,其原子结构示意图为
。
(3)元素的最高价氧化物对应的水化物中呈两性的氢氧化物是氢氧化铝,与氢氧化钠溶液反应的离子方程式是Al(OH)3+OH-=[Al(OH)4]-。
(4)同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则在②⑤⑦⑨四种元素中,原子半径由大到小的顺序是K>Si>Cl>F。
(5),同主族自上而下非金属性逐渐减弱,最高价氧化物对应水化物的酸性逐渐减弱,则元素⑥、⑩的最高价氧化物对应的水化物中,酸性较强的是H2SO4。
考点
据考高分专家说,试题“(9分)下表是元素周期表的一部分:针对表.....”主要考查你对 [构成物质的粒子—分子、原子、离子 ]考点的理解。
构成物质的粒子—分子、原子、离子
构成物质的微粒:
构成物质的粒子有分子、原子、离子
分子:能够独立存在并保持物质化学性质的一种微粒。
原子:化学变化中的最小粒子。
离子:带电荷的原子或原子团。
原子的构成:
(1)在原子中核电荷数=质子数=核外电子数决定元素种类质子数(核电荷数)
(2)原子的质量主要集中在原子核上
(3)三决定:质子数决定元素种类
最外层电子数决定化学性质
原子核决定原子的质量
(4)相对原子质量≈质子数+中子数
说明:最外层电子数相同其化学性质不一定都相同(Mg,He最外层电子数为2);最外层电子数不同其化学性质有可能相似(He,Ne均为稳定结构)
原子、分子、离子的区别与联系:
区别:
离子是原子或原子团由于得失电子而形成的带电微粒。
原子是化学变化中的最小微粒。
分子是物质中保持原物质的一切化学性质、能够独立存在的最小微粒。
联系:
分子是由原子组成的。在化学变化中,分子可再分,原子不可再分。分子是独立存在而保持物质化学性质的最小粒子。
原子、分子、离子的表示方法:
原子通常用表示,分子用化学式表示,离子用
表示。




