题文
设NA为阿伏加德罗常数,下列叙述正确的是 A.只有在标准状况下,气体的物质的量n与分子数N之间的关系 n = N/NA 才成立B.N2 (g)+3H2(g) 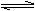
2NH3 (g) △H = -92.3kJ/mol,在该条件下,加入一定量的N2、H2发生反应转移6 NA e- 时,反应放出的热小于92.3 kJC.1mol/L 500mL氯化镁溶液中的镁离子数小于0.5NAD.常温下,1L pH =10的 CH3COONa溶液中因为CH3COO-的水解,将使OH-数大于10-4NA
题型:未知 难度:其他题型
答案
C
点击查看阿伏加德罗定律知识点讲解,巩固学习
解析
正确答案:C
A.不正确,在任何条件下,气体的物质的量n与分子数N之间的关系 n = N/NA 才成立
B.不正确,N2 (g)+3H2 (g) 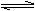
2NH3 (g) △H = -92.3kJ/mol,在该条件下,加入一定量的N2、H2 发生反应转移6 NA e- 时,反应放出的热等于92.3 kJ
C.正确,Mg2+要水解,1mol/L 500mL氯化镁溶液中的镁离子数小于0.5NA
D.不正确,常温下,1L pH =10的 CH3COONa溶液中,OH-数等于10-4NA
考点
据考高分专家说,试题“设NA为阿伏加德罗常数,下列叙述正确的是.....”主要考查你对 [阿伏加德罗定律 ]考点的理解。
阿伏加德罗定律
阿伏伽德罗定律:
同温同压下,相同体积的任何气体含有相同的分子数。
阿伏伽德罗定律的使用范围:
阿伏伽德罗定律只对气体起作用,使用于任何气体,包括混合气体。
方法与技巧:
- “三同”定“一同”(温度、压强、气体体积、气体分子数);“两同”定“比例”。
- 阿伏伽德罗定律及其推论的数学表达式可由理想气体状态方程(PV=nRT)或其变形形式(PM=ρRT)推出,不用死记硬背。
null
null
理想气体状态方程:
理想气体状态方程的表达式:PV= nRT
P表示压强,V 表示体积,T表示温度,R是常数,n是气体的物质的量。
可根据此方程来推断阿伏伽德罗定律的相关推论:
条件 结论 语言表达 T、P相同 n1/n2=V1/V2 同温同压下,气体的分子数与其体积成正比 T、V相同 n1/n2=P1/P2 同温同体积,压强与其分子数成正比 n、P相同 V1/V2=T1/T2 分子数、压强相同的气体,体积与温度成正比 n、T相同 P1/P2= V2/V1 分子数、温度相同的气体,压强与体积成反比 T、P相同 ρ1/ρ2=M1/M2 同温同压下,气体的密度与相对分子质量(摩尔质量)成正比 T、P、V相同 m1/m2=M1/M2 同温同压下,相同体积的气体,质量与其相对分子质量成正比 T、P、m相同 M1/M2=V2/V1 同温同压下,等质量的气体,相对分子质量与其体积成反比




