题文
某工厂的废水中只含氯化镁和少量盐酸,课外活动小组以此作为课题,探讨如何从中提取纯净的氯化镁固体.他们设计了两种不同的方案,请你参加讨论:
(1)方案一:选用镁粉为试剂.
往废水中逐次加入镁粉,当观察到______时,说明加入的镁粉的量已经足够,接下来的操作依次是______和______,从而得到氯化镁固体.
(2)方案二:选用氢氧化钠溶液为试剂向废水中逐滴加入氢氧化钠溶液,当观察到______时,停止滴入氢氧化钠溶液.为了得到纯净的氯化镁固体,接着进行的操作应该是______
(3)比较以上两个方案,假设实验中都没有损耗,那么通过以上两种方法得到的氯化镁的质量是否相同?______,理由是______.
(4)继续探究:请你设计新的方案,要求使用与镁和氢氧化钠不同类别的试剂,那么你想选用的试剂是______(填化学式)发生的化学反应方程式是______.
题型:未知 难度:其他题型
答案
(1)镁和盐酸反应生成氯化镁和氢气,氢气进入大气中,所以最后溶液中有固体镁(剩余)和氯化镁和水,过滤后滤液就是氯化镁溶液,然后蒸发把水蒸干得到氯化镁固体.故答案为:加入镁粉不再产生气泡,过滤,蒸发结晶.
(2)氯化镁和氢氧化钠反应生成氢氧化镁(沉淀)和氯化钠,盐酸和氢氧化钠生成氯化钠和水,所以经过过滤得到氢氧化镁沉淀.氢氧化镁和盐酸生成氯化镁和水,经过蒸发把水蒸干得到固体氯化镁.故答案为:白色沉淀不再增加 过滤后取滤渣加适量盐酸溶解,然后蒸发结晶.
(3)根据质量守恒定律可知,除原有的氯化镁之外,(1)中镁和盐酸反应也生成了氯化镁.故答案为:不同 因为在方案一中镁与盐酸反应会生成部分氯化镁,所以方案一比方案二中得到的氯化镁多一些.
(4)氧化镁和盐酸反应生成氯化镁和水,然后蒸发就可以得到固体氯化镁.故答案为:MgO,MgO+2HCl=MgCl2+H2O.
点击查看物质的相互转化和制备知识点讲解,巩固学习
解析
该题暂无解析
考点
据考高分专家说,试题“某工厂的废水中只含氯化镁和少量盐酸,课外.....”主要考查你对 [物质的相互转化和制备 ]考点的理解。
物质的相互转化和制备
物质的相互转化和制备:
主要是指以氧气、氢气、碳、硫、磷等为代表的非金属单质,以铝、镁、锌、铁、铜为代表的金属单质,以一氧化碳、二氧化碳等为代表的非金属氧化物,以氧化铜、氧化铁等为代表的金属氧化物,以盐酸、硫酸、碳酸等为代表的酸,以氢氧化钠、氢氧化钙等为代表的碱,以氯化钠、碳酸钠、碳酸氢钠、碳酸钙等为代表的盐,等等物质之间的相互和制备.
物质的相互转化:
氢氧化钠与氢氧化钙的制备:
(1)NaOH的制备
方法一:Na2O+H2O==2NaOH
方法二:Na2CO3+Ca(OH)2==CaCO3↓ +2NaOH
(2)Ca(OH)2的制备方法:CaO+H2O==Ca(OH)2
常见物质的相互转化:
Na→Na2O→NaOH→Na2CO3
C→CO→CO2→H2CO3
Fe→Fe2O3→Fe2(SO4)3→Fe(OH)3→FeCl3
S→SO2→SO3→H2SO4(单质硫不能直接转化为SO3)
各类物质间的转化关系:

(1)金属+
金属氧化物(碱性氧化物) 
(2)碱性氧化物(可溶)+水
碱(可溶)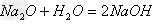
(3)碱(难溶)
碱氧(难溶)+水 
(4)酸+碱
盐+水 
;
(5)非金属+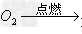
非金属氧化物(酸性氧化物)
(6)酸性氧化物(易溶)+水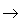
酸(易溶)
(7)酸(易挥发/难溶)
酸氧+水(易挥发/难溶) 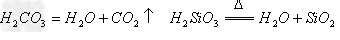
从纵向来看,金属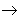
碱性氧化物
碱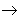
盐,其中金属元素相同。
非金属
酸性氧化物
酸(含氧酸)
盐,其中非金属元素相同。
横向:
(8)金属+非金属(无氧酸)
盐 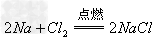
(9)碱氧+酸氧(含氧酸)
盐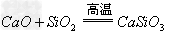
(10)含氧酸盐
碱氧+酸氧
(11)盐+盐
两种新盐 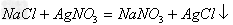
交叉:
(12)酸+碱氧
盐+水
(13)碱+酸氧
盐+水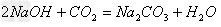
(14)酸+盐
新酸+新盐
;
(15)碱+盐
新碱+新盐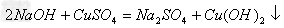
(16)金属+酸
盐+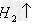

(17)金属+盐
新盐+新金属
(18)金属+盐
新盐+新金属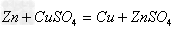
(置换反应)




