题文
已知:铁单质与高价铁盐溶液反应得亚铁盐溶液如2FeCl3+Fe=3FeCl2.某化学试剂厂产生废水中含有AgNO3和Fe(NO3)3,为防止污染环境,同时为了综合利用,回收其中的银,将Fe(NO3)3转化为FeSO4.7H2O,并能得到可灌溉农田的一种钾肥(KNO3溶液).某校“STS”小组与该厂科技人员合作,设计了如图所示的方案:
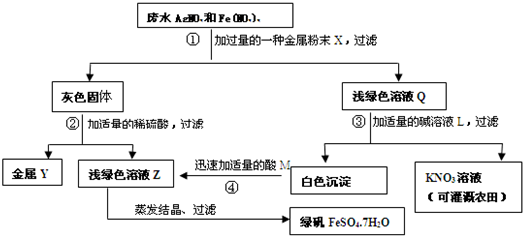
(1)试用化学式表示推断结果(若是溶液只写溶质的化学式)
Y______ Z______ L______
(2)按图标号写化学方程式:
②______ ④______.
题型:未知 难度:其他题型
答案
废水中加入金属X后得到了浅绿色的溶液Q和灰色固体,根据题中的信息可以判断浅绿色溶液Q为硝酸亚铁溶液,而灰色固体为铁和银的混合物,而铁可以和硫酸反应但是银不能,所以判断金属Y为银,而浅绿色溶液Z为硫酸亚铁溶液;根据题意为了得到硝酸钾,所以向溶液Q中加入的碱的溶液L应该为氢氧化钾溶液,即得到的白色沉淀为氢氧化亚铁,而反应中加入酸后得到了硫酸亚铁溶液,所以可以判断酸M为硫酸;
(1)根据上述分析可以知道Y为银,其化学式为Ag,溶液Z为硫酸亚铁溶液,其化学式为:FeSO4;溶液L为氢氧化钾溶液,其化学式为KOH;
(2)根据上述分析可以知道反应②为铁和硫酸的反应,该反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑;反应④为氢氧化亚铁和硫酸的反应,该反应的化学方程式为:H2SO4+Fe(OH)2═FeSO4 +2H2O;
故答案为:(1)Ag;FeSO4;KOH;
(2)Fe+H2SO4═FeSO4+H2↑;H2SO4+Fe(OH)2═FeSO4 +2H2O.
点击查看物质的相互转化和制备知识点讲解,巩固学习
解析
该题暂无解析
考点
据考高分专家说,试题“已知:铁单质与高价铁盐溶液反应得亚铁盐溶.....”主要考查你对 [物质的相互转化和制备 ]考点的理解。
物质的相互转化和制备
物质的相互转化和制备:
主要是指以氧气、氢气、碳、硫、磷等为代表的非金属单质,以铝、镁、锌、铁、铜为代表的金属单质,以一氧化碳、二氧化碳等为代表的非金属氧化物,以氧化铜、氧化铁等为代表的金属氧化物,以盐酸、硫酸、碳酸等为代表的酸,以氢氧化钠、氢氧化钙等为代表的碱,以氯化钠、碳酸钠、碳酸氢钠、碳酸钙等为代表的盐,等等物质之间的相互和制备.
物质的相互转化:
氢氧化钠与氢氧化钙的制备:
(1)NaOH的制备
方法一:Na2O+H2O==2NaOH
方法二:Na2CO3+Ca(OH)2==CaCO3↓ +2NaOH
(2)Ca(OH)2的制备方法:CaO+H2O==Ca(OH)2
常见物质的相互转化:
Na→Na2O→NaOH→Na2CO3
C→CO→CO2→H2CO3
Fe→Fe2O3→Fe2(SO4)3→Fe(OH)3→FeCl3
S→SO2→SO3→H2SO4(单质硫不能直接转化为SO3)
各类物质间的转化关系:

(1)金属+
金属氧化物(碱性氧化物) 
(2)碱性氧化物(可溶)+水
碱(可溶)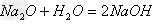
(3)碱(难溶)
碱氧(难溶)+水 
(4)酸+碱
盐+水 
;
(5)非金属+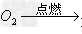
非金属氧化物(酸性氧化物)
(6)酸性氧化物(易溶)+水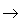
酸(易溶)
(7)酸(易挥发/难溶)
酸氧+水(易挥发/难溶) 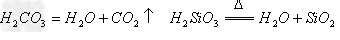
从纵向来看,金属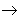
碱性氧化物
碱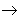
盐,其中金属元素相同。
非金属
酸性氧化物
酸(含氧酸)
盐,其中非金属元素相同。
横向:
(8)金属+非金属(无氧酸)
盐 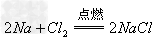
(9)碱氧+酸氧(含氧酸)
盐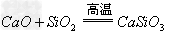
(10)含氧酸盐
碱氧+酸氧
(11)盐+盐
两种新盐 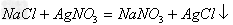
交叉:
(12)酸+碱氧
盐+水
(13)碱+酸氧
盐+水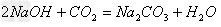
(14)酸+盐
新酸+新盐
;
(15)碱+盐
新碱+新盐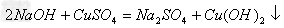
(16)金属+酸
盐+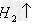

(17)金属+盐
新盐+新金属
(18)金属+盐
新盐+新金属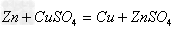
(置换反应)




