题文
高纯度硅(Si)是现代电子信息工业的关键材料,其制取原理如下图所示:

(1)原理中两次应用置换反应后,可以大大提高硅(Si)的纯度.置换反应在工业生产中具有重要的意义,通常置换反应可以用以下通式表示:单质+化合物═新单质+新化合物.根据已有知识及题目中的信息归纳完成表格:
单质类别新单质类别对应的置换反应的化学方程式(各举一例)A金属非金属______B金属另一种金属______C非金属金属______D____________SiO2+2C 高温、电炉 . Si+2CO↑(2)原理图中反应②的基本反应类型为______.试写出③的化学反应方程式______.
题型:未知 难度:其他题型
答案
(1)A.金属单质镁和稀盐酸反应能生成氯化镁和非金属单质氢气.故填:Mg+2HCl MgCl2+H2↑
B.金属单质铁和硫酸铜反应能生成硫酸亚铁和金属单质铜.故填:Fe+CuSO4=FeSO4+Cu.
C.非金属单质碳能和氧化铁反应生成二氧化碳和金属单质铁.故填:2Fe2O3+3C 高温 . 4Fe+3CO2↑
D.非金属单质碳能和二氧化硅反应生成一氧化碳和非金属单质硅.故填:非金属;非金属.
(2)硅和氯气反应生成四氯化硅,反应的化学方程式为:SiCl4+2H2 高温 . Si+4HCl.反应特点,是“多变一”,是化合反应
故答案为:化合反应;SiCl4+2H2 高温 . Si+4HCl
点击查看物质的相互转化和制备知识点讲解,巩固学习
解析
高温 .
考点
据考高分专家说,试题“高纯度硅(Si)是现代电子信息工业的关键.....”主要考查你对 [物质的相互转化和制备 ]考点的理解。
物质的相互转化和制备
物质的相互转化和制备:
主要是指以氧气、氢气、碳、硫、磷等为代表的非金属单质,以铝、镁、锌、铁、铜为代表的金属单质,以一氧化碳、二氧化碳等为代表的非金属氧化物,以氧化铜、氧化铁等为代表的金属氧化物,以盐酸、硫酸、碳酸等为代表的酸,以氢氧化钠、氢氧化钙等为代表的碱,以氯化钠、碳酸钠、碳酸氢钠、碳酸钙等为代表的盐,等等物质之间的相互和制备.
物质的相互转化:
氢氧化钠与氢氧化钙的制备:
(1)NaOH的制备
方法一:Na2O+H2O==2NaOH
方法二:Na2CO3+Ca(OH)2==CaCO3↓ +2NaOH
(2)Ca(OH)2的制备方法:CaO+H2O==Ca(OH)2
常见物质的相互转化:
Na→Na2O→NaOH→Na2CO3
C→CO→CO2→H2CO3
Fe→Fe2O3→Fe2(SO4)3→Fe(OH)3→FeCl3
S→SO2→SO3→H2SO4(单质硫不能直接转化为SO3)
各类物质间的转化关系:

(1)金属+
金属氧化物(碱性氧化物) 
(2)碱性氧化物(可溶)+水
碱(可溶)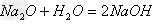
(3)碱(难溶)
碱氧(难溶)+水 
(4)酸+碱
盐+水 
;
(5)非金属+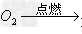
非金属氧化物(酸性氧化物)
(6)酸性氧化物(易溶)+水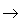
酸(易溶)
(7)酸(易挥发/难溶)
酸氧+水(易挥发/难溶) 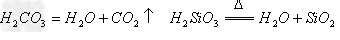
从纵向来看,金属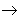
碱性氧化物
碱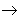
盐,其中金属元素相同。
非金属
酸性氧化物
酸(含氧酸)
盐,其中非金属元素相同。
横向:
(8)金属+非金属(无氧酸)
盐 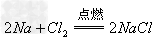
(9)碱氧+酸氧(含氧酸)
盐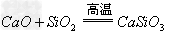
(10)含氧酸盐
碱氧+酸氧
(11)盐+盐
两种新盐 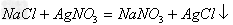
交叉:
(12)酸+碱氧
盐+水
(13)碱+酸氧
盐+水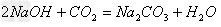
(14)酸+盐
新酸+新盐
;
(15)碱+盐
新碱+新盐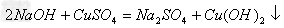
(16)金属+酸
盐+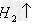

(17)金属+盐
新盐+新金属
(18)金属+盐
新盐+新金属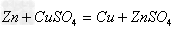
(置换反应)




