题文
追踪科学家的足迹
材料1:纯碱的产量是衡量一个国家化学工业发展水平的重要指标.下面是实验室摸拟侯氏制碱法生产原理的主要过程:
(1)20℃时,向浓氨水中通入足量的二氧化碳得到NH4HCO3饱和溶液;
②向NH4HCO3饱和溶液中加入食盐细粒,并不断搅拌,直到NaHCO3结晶析出完毕;
③将析出的晶体过滤,得到晶体和滤液,洗涤晶体,然后将晶体放在试管中充分加热,得到Na2CO3;
④向③的滤液中加入食盐细粒,析出NH4CI晶体,过滤,得到NH4CI.
材料2:四种盐在不同温度下的溶解度表.
温度
盐
溶解度10℃20℃30℃40℃50℃NaCl35.836.036.336.637.0NH4HCO315.821.027.0------------NaHCO38.19.611.112.7----NH4Cl33.337.241.445.850.4试回答下列问题:
(1)在实验室中,你选择的制备C02反应的化学方程式为______.在工业生产中,要获得生产纯碱的原料CO2你认为最经济实用的方法是以______为原料,该反应的化学方程式为______.
(2)有人认为侯氏制碱法有以下优点,你认为其中正确的是______.
A.生产过程中部分反应产物可作为原料循环使用
B.副产品是一种氮肥
C.反应都不需要加热,可节约能源
(3)检验③中的白色粉末中是否含有氯化钠的方法是______.
(4)在②中,随着食盐的逐渐加入,溶液变成了NH4HCO3和NaCl的混合溶液,析出晶体之前,混合溶液中存在的离子有(用离子符号表示,下同.)______.在③中,将析出的晶体过滤后,溶液中数量减少的离子有______;滤液中仍然存在的离子有______.②中反应的化学方程式为______.
(5)在20℃时,向含NH4HC0321g的饱和溶液中加入足量食盆.试通过计算说明,随着食盐的逐渐加入,为什么会有NaHC03晶体析出,而没有NH4Cl.
题型:未知 难度:其他题型
答案
(1)实验室制二氧化碳要求纯度高,便于收集,一般用石灰石或大理石(主要成分是碳酸钙)与稀盐酸反应,生成氯化钙、水、二氧化碳,方程式为:CaC03+2HCl=CaCl2+CO2↑+H2O;工业生产中需二氧化碳对纯度要求不高,但要考虑成本和是否能大量生产,所以用高温煅烧石灰石的方法,方程式为:CaCO3 高温 . CaO+CO2↑.
(2)A、生产过程步骤④得到的氯化钠溶液可作为步骤②制碳酸氢钠的原料循环使用,所以正确.
B、副产品是氯化铵,其中含有氮元素,是一种氮肥,所以正确.
C、步骤③碳酸氢钠分解制纯碱时需要加热,所以错误.
(3)检验③中的白色粉末中是否含有氯化钠,实际上是检验氯离子的存在,方法为:取③中色粉末少许于试管中加入稀硝酸化,再滴入硝酸银溶液,若不产生生白色沉淀证明不含氯化钠,反之则含氯化钠.
(4)在NH4HCO3和NaCl的混合溶液中,前者是以NH4+、HCO3-形式存在的,后者是以Na+、C1-形式存在的,所以溶液中含有的离子是NH4+、HCO3-、Na+、C1-;在③中,碳酸氢钠析出,将析出的晶体过滤后,溶液中数量减少的离子是碳酸氢钠电离出来的,有HCO3-、Na+;由碳酸氢钠是饱和后才析出的,滤液中仍然存在部分碳酸氢钠,溶液中含有的离子有NH4+、HCO3-、Na+、C1-;②中碳酸氢钠析出,可看作是生成了沉淀,是碳酸氢铵和氯化钠发生了复分解反应,方程式为:NH4HCO3+NaCl=NH4Cl+NaHCO3↓.
(5)设21gNH4HCO3完全转化能生成NaHCO3的质量为x,能生成NH4Cl的质量为y
NH4HCO3+NaCl═NH4Cl+NaHCO3
79 53.5 84
21g y x
X=22.3g
Y=14.2g
根据四种物质的溶解度,20℃时,1OOg水最多能溶解9.6gNaHCO3,37.2gNH4Cl.因为22.3>9.6g,所以有NaHC03析出.
理论上可析出NaHC03的质量:22.3g-9.6g=12.7g,因为14.2g<37.2g,NH4Cl没有达到饱和状态,所以不可能有NH4Cl析出.
故答案为:
(1)CaC03+2HCl=CaCl2+CO2↑+H2O;石灰石;CaCO3 高温 . CaO+CO2↑;
(2)AB;
(3)取③中色粉末少许于试管中加入稀硝酸化,再滴入硝酸银溶液,若不产生生白色沉淀证明不含氯化钠,反之则含氯化钠;
(4)NH4+、HCO3-、Na+、C1-;HCO3-、Na+;NH4+、HCO3-、Na+、Cl-;NH4HCO3+NaCl=NH4Cl+NaHCO3↓;
(5)设21gNH4HCO3完全转化能生成NaHCO3的质量为x,能生成NH4Cl的质量为y
NH4HCO3+NaCl═NH4Cl+NaHCO3
79 53.5 84
21g y x
X=22.3g
Y=14.2g
根据四种物质的溶解度,20℃时,1OOg水最多能溶解9.6gNaHCO3,37.2gNH4Cl.因为22.3>9.6g,所以有NaHC03析出.
理论上可析出NaHC03的质量:22.3g-9.6g=12.7g,因为14.2g<37.2g,NH4Cl没有达到饱和状态,所以不可能有NH4Cl析出.
点击查看物质的相互转化和制备知识点讲解,巩固学习
解析
高温 .
考点
据考高分专家说,试题“追踪科学家的足迹材料1:纯碱的产量是衡量.....”主要考查你对 [物质的相互转化和制备 ]考点的理解。
物质的相互转化和制备
物质的相互转化和制备:
主要是指以氧气、氢气、碳、硫、磷等为代表的非金属单质,以铝、镁、锌、铁、铜为代表的金属单质,以一氧化碳、二氧化碳等为代表的非金属氧化物,以氧化铜、氧化铁等为代表的金属氧化物,以盐酸、硫酸、碳酸等为代表的酸,以氢氧化钠、氢氧化钙等为代表的碱,以氯化钠、碳酸钠、碳酸氢钠、碳酸钙等为代表的盐,等等物质之间的相互和制备.
物质的相互转化:
氢氧化钠与氢氧化钙的制备:
(1)NaOH的制备
方法一:Na2O+H2O==2NaOH
方法二:Na2CO3+Ca(OH)2==CaCO3↓ +2NaOH
(2)Ca(OH)2的制备方法:CaO+H2O==Ca(OH)2
常见物质的相互转化:
Na→Na2O→NaOH→Na2CO3
C→CO→CO2→H2CO3
Fe→Fe2O3→Fe2(SO4)3→Fe(OH)3→FeCl3
S→SO2→SO3→H2SO4(单质硫不能直接转化为SO3)
各类物质间的转化关系:

(1)金属+
金属氧化物(碱性氧化物) 
(2)碱性氧化物(可溶)+水
碱(可溶)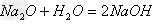
(3)碱(难溶)
碱氧(难溶)+水 
(4)酸+碱
盐+水 
;
(5)非金属+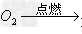
非金属氧化物(酸性氧化物)
(6)酸性氧化物(易溶)+水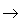
酸(易溶)
(7)酸(易挥发/难溶)
酸氧+水(易挥发/难溶) 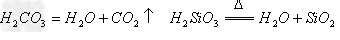
从纵向来看,金属
碱性氧化物
碱
盐,其中金属元素相同。
非金属
酸性氧化物
酸(含氧酸)
盐,其中非金属元素相同。
横向:
(8)金属+非金属(无氧酸)
盐 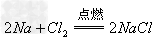
(9)碱氧+酸氧(含氧酸)
盐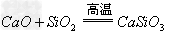
(10)含氧酸盐
碱氧+酸氧
(11)盐+盐
两种新盐 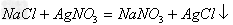
交叉:
(12)酸+碱氧
盐+水
(13)碱+酸氧
盐+水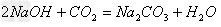
(14)酸+盐
新酸+新盐
;
(15)碱+盐
新碱+新盐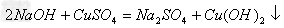
(16)金属+酸
盐+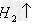

(17)金属+盐
新盐+新金属
(18)金属+盐
新盐+新金属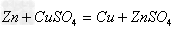
(置换反应)




