题文
自然界的矿物中有一种重晶石矿的主要成分是BaSO4,它不溶于任何酸、碱和水,纯净的硫酸钡可供医疗等方面应用,某同学用重晶石和焦炭为原料,制取纯净硫酸钡,部分流程如下(设矿物中杂质不与焦炭反应,也不溶于水):
(1)步骤①中,哪些元素的化合价升高,哪些元素化合价降低?______,
(2)步骤②中溶液A中溶质的化学式:______;
(3)写出利用溶液A中的溶质为主要原料制取BaSO4的化学方程式:______.
(4)步骤②产生有毒气体H2S,应加以改进,为使实验既不产生H2S又能获得纯净BaSO4,请你提出改进意见.______;
有关反应的化学方程式是______.
题型:未知 难度:其他题型
答案
(1)杂质不参与反应,因此不考虑杂质中的元素;而反应前BaSO4与C中Ba、S、O、C元素的化合价分别为+2、+6、-2、0,反应后BaS、CO中Ba、S、O、C元素的化合价分别为+2、-2、-2、+2,因此可判断碳元素化合价由0升高至+2,而硫元素的化合价由+6降低至-2;
(2)硫化钡与盐酸反应生成硫化氢气体,可判断反应的化学方程式为BaS+2HCl=BaCl2+H2S↑,因此该步反应中所得溶液A中溶质为氯化钡,其化学式为BaCl2;
(3)利用氯化钡能与硫酸钠等发生复分解反应生成硫酸钡的氯化钠的转化关系,可使用氯化钡与硫酸钠反应,反应的化学方程式为BaCl2+Na2SO4=BaSO4↓+2NaCl;
(4)利用硫化钡这种盐与可溶解性硫酸盐能生成硫酸钡和另一种盐,既可避免与盐酸反应放出有毒气体硫化氢又可直接转化为硫酸钡,因此可采取在步骤②中加入硫酸钠,反应后过滤并洗涤除去附在固体表面的溶液,得到较为纯净的硫酸钡,反应的化学方程式为BaS+Na2SO4=BaSO4↓+Na2S;
故答案为:
(1)碳元素化合价升高,硫元素化合价降低;
(2)BaCl2;
(3)BaCl2+Na2SO4=BaSO4↓+2NaCl;
(4)可在步骤②中加入Na2SO4,然后过滤,洗涤后可得纯净BaSO4; BaS+Na2SO4=BaSO4↓+Na2S.
点击查看物质的相互转化和制备知识点讲解,巩固学习
解析
该题暂无解析
考点
据考高分专家说,试题“自然界的矿物中有一种重晶石矿的主要成分是.....”主要考查你对 [物质的相互转化和制备 ]考点的理解。
物质的相互转化和制备
物质的相互转化和制备:
主要是指以氧气、氢气、碳、硫、磷等为代表的非金属单质,以铝、镁、锌、铁、铜为代表的金属单质,以一氧化碳、二氧化碳等为代表的非金属氧化物,以氧化铜、氧化铁等为代表的金属氧化物,以盐酸、硫酸、碳酸等为代表的酸,以氢氧化钠、氢氧化钙等为代表的碱,以氯化钠、碳酸钠、碳酸氢钠、碳酸钙等为代表的盐,等等物质之间的相互和制备.
物质的相互转化:
氢氧化钠与氢氧化钙的制备:
(1)NaOH的制备
方法一:Na2O+H2O==2NaOH
方法二:Na2CO3+Ca(OH)2==CaCO3↓ +2NaOH
(2)Ca(OH)2的制备方法:CaO+H2O==Ca(OH)2
常见物质的相互转化:
Na→Na2O→NaOH→Na2CO3
C→CO→CO2→H2CO3
Fe→Fe2O3→Fe2(SO4)3→Fe(OH)3→FeCl3
S→SO2→SO3→H2SO4(单质硫不能直接转化为SO3)
各类物质间的转化关系:

(1)金属+
金属氧化物(碱性氧化物) 
(2)碱性氧化物(可溶)+水
碱(可溶)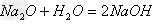
(3)碱(难溶)
碱氧(难溶)+水 
(4)酸+碱
盐+水 
;
(5)非金属+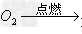
非金属氧化物(酸性氧化物)
(6)酸性氧化物(易溶)+水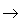
酸(易溶)
(7)酸(易挥发/难溶)
酸氧+水(易挥发/难溶) 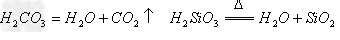
从纵向来看,金属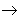
碱性氧化物
碱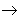
盐,其中金属元素相同。
非金属
酸性氧化物
酸(含氧酸)
盐,其中非金属元素相同。
横向:
(8)金属+非金属(无氧酸)
盐 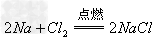
(9)碱氧+酸氧(含氧酸)
盐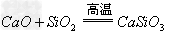
(10)含氧酸盐
碱氧+酸氧
(11)盐+盐
两种新盐 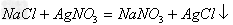
交叉:
(12)酸+碱氧
盐+水
(13)碱+酸氧
盐+水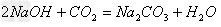
(14)酸+盐
新酸+新盐
;
(15)碱+盐
新碱+新盐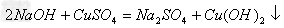
(16)金属+酸
盐+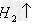

(17)金属+盐
新盐+新金属
(18)金属+盐
新盐+新金属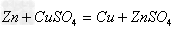
(置换反应)




