题文
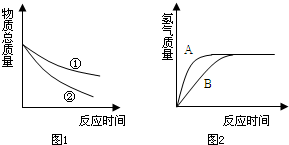
小红和小明进行盐酸与锌反应制取氢气的实验研究.小红用较稀的盐酸,小明用较浓的盐酸.他们分别取等质量的锌粒与等质量盐酸在烧杯中反应,(假设盐酸均足量)并将烧杯中物质总质量随反应时间的变化情况绘制成图1.
试回答下列问题:
(1)烧杯中物质总质量减少的原因是______;
(2)表示小红实验结果的是图中的曲线______(填①或②);
(3)请说明图中的曲线②与曲线①不同的原因______.
(4)图2是小李同学绘制的小红与小明各自实验中产生纯氢气随时间变化的情况,请指出表示小明实验的曲线是______(填“A”或“B”)
题型:未知 难度:其他题型
答案
(1)锌能与盐酸反应生成氢气逸出、盐酸具有挥发性、反应放热导致水分蒸发,从而使烧杯内物质的总质量减小.故答案为:反应放出氢气、氯化氢气体逸出、反应放热导致水分蒸发;
(2)小红用的是稀盐酸,反应较慢,相同时间内生成氢气较少;稀盐酸挥发性较小.因此相同时间内烧杯内物质的总质量比用浓盐酸时剩余的多.表现在图象上就是锌与稀盐酸反应的曲线比与浓盐酸的高.故答案为:①;
(3)图中的曲线②与曲线①不同的原因是:曲线②浓盐酸,浓度较大,逸出的氯化氢气体多;并且与锌反应速度较快,曲线下降快,故其质量减小较快;故答案为:a.曲线②盐酸浓度较大,反应速率较快,所以曲线下降较快b.曲线②盐酸浓度较大,逸出的氯化氢气体多,所以最后位置较低;
(4)因为小明用的是浓盐酸,反应速率快,比小红的实验用的时间少.故填:A
点击查看氢气的制取和收集知识点讲解,巩固学习
解析
该题暂无解析
考点
据考高分专家说,试题“小红和小明进行盐酸与锌反应制取氢气的实验.....”主要考查你对 [氢气的制取和收集 ]考点的理解。
氢气的制取和收集
实验室里通常用稀硫酸跟金属锌起反应来制取氢气,也可以用盐酸代替硫酸,用镁或铁代替锌来制取氢气。
氢气的实验室制法:
化学药品锌粒和稀硫酸反应原理Zn + H2SO4== ZnSO4+ H2↑ 发生装置反应物状态为固态和液态,反应条件为室温,可选择实验室制CO2的反应装置(或用过氧化氢溶液制氧气的反应装置)
收集装置向下排空气法或排水法

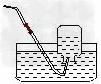
实验步骤①检验装置的气密性
②装锌粒(注意将试管横放,把锌粒放入试管口,再慢慢竖起)
③把试管固定在铁架台上
④加入稀硫酸
⑤收集气体 注意事项①不能用浓H2SO4代替稀H2SO4,浓H2SO4具有强氧化性
②不能用金属活动性顺序表中排在氢后面的金属,如铜,也不能用排在氢前的金属,如钠,一般常用Zn、Al、Fe、Mg等。
③长颈漏斗末端应在液而以下,防止氢气从长颈漏斗逸出
氢气的工业制法:
制取方法原理优缺点电解水2H2O
2H2↑+O2优点:得到氢气纯度高
缺点:耗能高 水煤气C+H2O(g)
CO+H2优点:成本低
缺点:需要设备多(需要除去CO中的杂质) 天然气CH4
C+2H2优点:原料丰富
缺点:氢气纯度低 电解饱和食盐水2NaCl+2H2O
2NaOH+H2↑+Cl2↑优点:是氯碱化工的副产品
缺点:纯度低 理想模式:利用太阳能、高效催化剂分解水2H2O
2H2↑+O2↑优点:不耗费电能、热能,环保
缺点:人类未能寻找到高效催化剂,还未能实际应用