题文
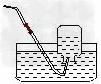
用如图装置制取氢气,在多孔塑料板上放锌粒,稀H2SO4由漏斗中加入.若打开弹簧夹,酸液由漏斗
中流下与锌粒接触即发生反应,产生的氢气由支管导出,请回答下列问题:
(1)发生反应的化学方程式为______.
(2)检查此装置的气密性时,关闭弹簧夹,从漏斗注入适量的水形成液封后,若看到漏斗内______,则表明装置气密性良好.
(3)反应过程中关闭弹簧夹,容器内继续反应产生的氢气会使容器内______,将酸液压回漏斗中,使酸液与锌粒______,反应即自行停止.
(4)若在塑料隔板上放小块大理石,漏斗中加入稀HCl,______(填能活否)用弹簧夹控制CO2的发生和停止.
题型:未知 难度:其他题型
答案
(1)锌能与稀硫酸反应生成硫酸锌和氢气,故填:Zn+H2SO4═ZnSO4+H2↑;
(2)检查此装置的气密性时,关闭弹簧夹,从漏斗注入适量的水形成液封后,若看到漏斗内液面不下降,则表明装置气密性良好,故填:液面不下降;
(3)反应过程中关闭弹簧夹,容器内继续反应产生的氢气会使容器内压强增大,将酸液压回漏斗中,使酸液与锌粒分离,反应即自行停止,故填:压强增大,分离;
(4)若在塑料隔板上放小块大理石,漏斗中加入稀HCl,盐酸与碳酸钙反应生成二氧化碳,能用弹簧夹控制CO2的发生和停止,故填:能.
点击查看氢气的制取和收集知识点讲解,巩固学习
解析
该题暂无解析
考点
据考高分专家说,试题“用如图装置制取氢气,在多孔塑料板上放锌粒.....”主要考查你对 [氢气的制取和收集 ]考点的理解。
氢气的制取和收集
实验室里通常用稀硫酸跟金属锌起反应来制取氢气,也可以用盐酸代替硫酸,用镁或铁代替锌来制取氢气。
氢气的实验室制法:
化学药品锌粒和稀硫酸反应原理Zn + H2SO4== ZnSO4+ H2↑ 发生装置反应物状态为固态和液态,反应条件为室温,可选择实验室制CO2的反应装置(或用过氧化氢溶液制氧气的反应装置)
收集装置向下排空气法或排水法

实验步骤①检验装置的气密性
②装锌粒(注意将试管横放,把锌粒放入试管口,再慢慢竖起)
③把试管固定在铁架台上
④加入稀硫酸
⑤收集气体 注意事项①不能用浓H2SO4代替稀H2SO4,浓H2SO4具有强氧化性
②不能用金属活动性顺序表中排在氢后面的金属,如铜,也不能用排在氢前的金属,如钠,一般常用Zn、Al、Fe、Mg等。
③长颈漏斗末端应在液而以下,防止氢气从长颈漏斗逸出
氢气的工业制法:
制取方法原理优缺点电解水2H2O
2H2↑+O2优点:得到氢气纯度高
缺点:耗能高 水煤气C+H2O(g)
CO+H2优点:成本低
缺点:需要设备多(需要除去CO中的杂质) 天然气CH4
C+2H2优点:原料丰富
缺点:氢气纯度低 电解饱和食盐水2NaCl+2H2O
2NaOH+H2↑+Cl2↑优点:是氯碱化工的副产品
缺点:纯度低 理想模式:利用太阳能、高效催化剂分解水2H2O
2H2↑+O2↑优点:不耗费电能、热能,环保
缺点:人类未能寻找到高效催化剂,还未能实际应用





