题文
为了制取干燥的CO2并进行有关实验,采用下列实验装置,请回答以下问题: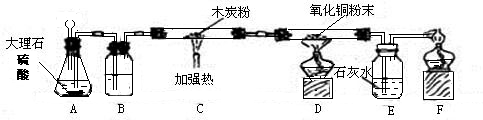
(1)作为CO2发生器的装置A中有______处错误,经改正后,该装置中发生的反应的化学方程式为______.
(2)装置B中装的物质通常是______.
(3)装置C中发生的化学方程式为______.
(4)装置D在实验中,观察到的主要现象是______.
(5)装置E的作用是______.
(6)装置F中为何要将尾气点燃?______.
题型:未知 难度:其他题型
答案
(1)制备CO2不能用硫酸和碳酸钙反应制备,因为稀硫酸和石灰石反应生成微溶于水的硫酸钙,覆盖在石灰石表面阻止反应;长颈漏斗使用时要将低端插入液面以下,以防生成的气体逸出;右边的导气管不能插入液面下.所以共有3处错误.发生的反应为:CaCO3+2HCl=CaCl2+CO2↑+H2O
(2)因为C装置中发生的是高温下反应,所以要求进入的反应物必须是干燥,否则玻璃管会破裂,所以B装置中应装浓硫酸,起干燥作用.
(3)用来制备CO气体,方程式为 C+CO2 高温 . 2CO
(4)D装置中发生的反应为:CuO+CO 加热 . Cu+CO2,黑色的氧化铜生成了红色的铜.
(5)E装置发生的反应为Ca(OH)2+CO2=CaCO3↓+H2O,所以E装置的作用是吸收CO2
(6)应为反应过程中CO不会全部反应,排入空气会污染大气,通常采用的方法是收集或点燃.
故填:(1)3;CaCO3+2HCl=CaCl2+CO2↑+H2O
(2)浓硫酸;
(3)C+CO2 高温 . 2CO;
(4)黑色粉末逐渐变为红色粉末;
(5)吸收CO2
(6)防止反应过程中产生的过量CO排放到空气中造成污染
点击查看二氧化碳的制取和收集知识点讲解,巩固学习
解析
高温 .
考点
据考高分专家说,试题“为了制取干燥的CO2并进行有关实验,采用.....”主要考查你对 [二氧化碳的制取和收集 ]考点的理解。
二氧化碳的制取和收集
二氧化碳的制取和收集:
1.原理和药品:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑
2.装置:固液混合不加热
(1)发生装置

A装置为简易装置,不便于加液体;
B,C使用了长颈漏斗,便于添加液体,使用B、C装置时应注意,长颈漏斗下端管日应伸入液面以下,防止产生的气体从长颈漏斗逸出;
D装置使用了分液漏斗,便于加酸,还可以利用活塞控制反应。
(2)收集装置:二氧化碳溶于水,所以不能用排水法收集;其密度比空气大,所以可采用向上排空气法收集。
如图: 
3.现象:块状固体不断溶解,产生大量气泡。
4.检验:把产生的气体通入澄清石灰水,若澄清石灰水变浑浊,证明是二氧化碳。
5.验满:将燃着的木条放在集气瓶口,如果木条的火焰熄灭,证明已集满。
6.实验步骤
a.检查装置的气密性;
b.装入石灰石(或大理石);
c. 塞紧双孔塞;
d.从长颈漏斗中加入稀盐酸;
e.收集气体;
f.验满。
7.注意事项:反应物不能用浓盐酸、硫酸、因为浓盐酸易挥发,会挥发出氯化氢气体,使制得的二氧化碳不纯;硫酸不会挥发,但会生成硫酸钙沉淀,沉淀的硫酸根附着在碳酸钙(或石灰石)表面,使碳酸钙(或石灰石)与酸的接触面积变小,最后反应停止!
实验室制取二氧化碳的选择:
实验室用大理石或石灰石(主要成分是碳酸钙)和稀盐酸制取二氧化碳。
注意:
(1)不能选用稀硫酸,因为稀硫酸与碳酸钙反应生成微溶于水的硫酸钙会橙盖在碳酸钙的表面,阻止反应继续进行。
(2)不能选用浓盐酸,因为浓盐酸易挥发,得不到纯净的二氧化碳气体。
(3)不能用碳酸钠代替石灰石,因为反应太剧烈,产生的气体难以收集。反应速率的快慢与反应物的质量分数和接触面积有关。反应物的接触面积越大,反应物的质量分数越大,反应速率就越快,反之,则越慢。
各组物质反应情况如下表所示:
药品反应速率块状石灰石和稀盐酸产生气泡速率适中石灰石粉末和稀盐酸产生气泡速率很快块状石灰石和稀硫酸产生气泡速率缓慢并逐渐停止碳酸钠粉末和稀盐酸产生气泡速率很快




