题文
(1)请从下列物质中选择适当的物质填空(不可重复选择):A.蛋白质;B.食盐;C.干冰;D.熟石灰;E.碳酸钠;F.硝酸钾(均填字母序号)。①厨房中用作调味品的是 ;②可用于人工降雨的是 ;
③牛奶中的主要营养物质是 ; ④常用于去除油渍的是 ;
⑤常用作改良酸性土壤的是 ;⑥可用作复合化肥的是 。
(2)填写专业术语名称
①二氧化锰在过氧化氢溶液分解制取氧气中作为 ;
②活性炭用于净水,是利用其中 性;
③洗涤精在清洗油污中起 作用;
④分离液体中混有的不溶性固体杂质通常采用 ;
⑤海水晒盐的道理实际上是 结晶;
⑥通常采用的高温消毒原理是,在高温下蛋白质发生 。
(3)在右图的虚线框内,用短线将装置的上下两部分相匹配的连接。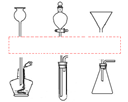
题型:未知 难度:其他题型
答案
(1)①B ②C ③A ④E ⑤D ⑥F
(2) ①催化剂 ②吸附 ③乳化 ④过滤 ⑤蒸发 ⑥变性
(3)
点击查看二氧化碳的制取和收集知识点讲解,巩固学习
解析
(1)①厨房中用作调味品的是食盐,②可用于人工降雨的是干冰,③牛奶中的主要营养物质是蛋白质,④常用于去除油渍的是碳酸钠,碳酸钠水溶液呈碱性,可用来除去油污,⑤常用作改良酸性土壤的是熟石灰,⑥可用作复合化肥的是硝酸钾,可同时提供钾元素和氮元素;(2)①二氧化锰在过氧化氢溶液分解制取氧气中作为催化剂,②活性炭疏松多孔,可以吸收杂质分子,可用于净水,③洗涤精可以乳化油污使之容易除去,④分离液体中混有的不溶性固体杂质通常采用过滤操作,⑤海水晒盐本质是蒸发结晶,⑥通常采用的高温消毒原理是,在高温下蛋白质发生变性。
点评:考察生活中常见现象里的化学知识,较简单,但是却是中考中的必考题,平时注意积累总结。
考点
据考高分专家说,试题“(1)请从下列物质中选择适当的物质填空(.....”主要考查你对 [二氧化碳的制取和收集 ]考点的理解。
二氧化碳的制取和收集
二氧化碳的制取和收集:
1.原理和药品:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑
2.装置:固液混合不加热
(1)发生装置

A装置为简易装置,不便于加液体;
B,C使用了长颈漏斗,便于添加液体,使用B、C装置时应注意,长颈漏斗下端管日应伸入液面以下,防止产生的气体从长颈漏斗逸出;
D装置使用了分液漏斗,便于加酸,还可以利用活塞控制反应。
(2)收集装置:二氧化碳溶于水,所以不能用排水法收集;其密度比空气大,所以可采用向上排空气法收集。
如图: 
3.现象:块状固体不断溶解,产生大量气泡。
4.检验:把产生的气体通入澄清石灰水,若澄清石灰水变浑浊,证明是二氧化碳。
5.验满:将燃着的木条放在集气瓶口,如果木条的火焰熄灭,证明已集满。
6.实验步骤
a.检查装置的气密性;
b.装入石灰石(或大理石);
c. 塞紧双孔塞;
d.从长颈漏斗中加入稀盐酸;
e.收集气体;
f.验满。
7.注意事项:反应物不能用浓盐酸、硫酸、因为浓盐酸易挥发,会挥发出氯化氢气体,使制得的二氧化碳不纯;硫酸不会挥发,但会生成硫酸钙沉淀,沉淀的硫酸根附着在碳酸钙(或石灰石)表面,使碳酸钙(或石灰石)与酸的接触面积变小,最后反应停止!
实验室制取二氧化碳的选择:
实验室用大理石或石灰石(主要成分是碳酸钙)和稀盐酸制取二氧化碳。
注意:
(1)不能选用稀硫酸,因为稀硫酸与碳酸钙反应生成微溶于水的硫酸钙会橙盖在碳酸钙的表面,阻止反应继续进行。
(2)不能选用浓盐酸,因为浓盐酸易挥发,得不到纯净的二氧化碳气体。
(3)不能用碳酸钠代替石灰石,因为反应太剧烈,产生的气体难以收集。反应速率的快慢与反应物的质量分数和接触面积有关。反应物的接触面积越大,反应物的质量分数越大,反应速率就越快,反之,则越慢。
各组物质反应情况如下表所示:
药品反应速率块状石灰石和稀盐酸产生气泡速率适中石灰石粉末和稀盐酸产生气泡速率很快块状石灰石和稀硫酸产生气泡速率缓慢并逐渐停止碳酸钠粉末和稀盐酸产生气泡速率很快




