题文
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
(1)“低碳生活”倡导低能量、低消耗,主要是为了减少 (填化学式)的排放量.
(2)如图所示
为元素周期表中的一格,下列说法不正确的是 (填标号).A.碳元素属于非金属元素B.碳原子核内质子数为6C.碳元素的原子结构示意图为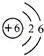
;D.碳的相对原子质量为12.01(3)为了探究二氧化碳能与水发生反应生成酸,小明设计了如下实验方案:
取四朵用石蕊试液染成紫色的干燥小花,按图中的步骤I~Ⅳ依次进行实验,观察小花的颜色变化 (资料:紫色石蕊试液遇酸变红色).
①该方案中观察到纸花的颜色变化是:I.纸花变红Ⅱ.纸花不变红Ⅲ. Ⅳ.
②步骤I、Ⅱ两项说明了什么? .
③该同学进行四组对比实验的目的是什么?
④写出该实验中所发生反应的化学方程式
(4)计算要使80g氧化铜完全还原,需要碳的质量至少是多少?
题型:未知 难度:其他题型
答案
(1)CO2; (2)C;(3)①纸花不变红;纸花变红;②说明了酸能使紫色石蕊变红,而水不能使紫色石蕊变红;③证明使紫色石蕊变红的不是二氧化碳本身,而是由二氧化碳与水反应生成的碳酸; ④CO2+H2O=H2CO3;(4)需要碳的质量至少为6g.
点击查看二氧化碳的制取和收集知识点讲解,巩固学习
解析
(1)“低碳生活”就是减少CO2的排放量;(2)A、因碳的偏旁为“石”,则碳元素为非金属元素,故A说法正确;B、由信息可知,碳原子的质子数为6,故B说法正确;C、碳原子的质子数为6,则原子结构中最外层电子数应为4,故C说法错误;D、由信息可知,碳原子的相对原子质量为12.01,故D说法正确;(3)①步骤III中存在二氧化碳气体,二氧化碳不具备酸性,所以纸花不会变红;步骤IV中纸花喷水后放入盛有二氧化碳的集气瓶,则水与二氧化碳会生成碳酸,碳酸会使石蕊变红,所以纸花变红;②步骤I中,醋酸显酸性,能使纸花变红.说明了酸能使紫色石蕊变红,步骤Ⅱ中向纸花上喷水,纸花不变色,说明了水不能使紫色石蕊变红;③该同学进行四组对比实验的目的是证明使紫色石蕊变红的不是二氧化碳本身,而是由二氧化碳与水反应生成的碳酸;④在该实验中二氧化碳与水化合生成了碳酸,反应的方程式是:CO2+H2O=H2CO3;
(4)解:设需要碳的质量至少为x.
C+2CuO
2Cu+CO2↑
12 160
x 80g
解得:x=6g
答:需要碳的质量至少为6g.
考点
据考高分专家说,试题“碳是形成化合物种类最多的元素,含碳物质是.....”主要考查你对 [二氧化碳的制取和收集 ]考点的理解。
二氧化碳的制取和收集
二氧化碳的制取和收集:
1.原理和药品:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑
2.装置:固液混合不加热
(1)发生装置

A装置为简易装置,不便于加液体;
B,C使用了长颈漏斗,便于添加液体,使用B、C装置时应注意,长颈漏斗下端管日应伸入液面以下,防止产生的气体从长颈漏斗逸出;
D装置使用了分液漏斗,便于加酸,还可以利用活塞控制反应。
(2)收集装置:二氧化碳溶于水,所以不能用排水法收集;其密度比空气大,所以可采用向上排空气法收集。
如图: 
3.现象:块状固体不断溶解,产生大量气泡。
4.检验:把产生的气体通入澄清石灰水,若澄清石灰水变浑浊,证明是二氧化碳。
5.验满:将燃着的木条放在集气瓶口,如果木条的火焰熄灭,证明已集满。
6.实验步骤
a.检查装置的气密性;
b.装入石灰石(或大理石);
c. 塞紧双孔塞;
d.从长颈漏斗中加入稀盐酸;
e.收集气体;
f.验满。
7.注意事项:反应物不能用浓盐酸、硫酸、因为浓盐酸易挥发,会挥发出氯化氢气体,使制得的二氧化碳不纯;硫酸不会挥发,但会生成硫酸钙沉淀,沉淀的硫酸根附着在碳酸钙(或石灰石)表面,使碳酸钙(或石灰石)与酸的接触面积变小,最后反应停止!
实验室制取二氧化碳的选择:
实验室用大理石或石灰石(主要成分是碳酸钙)和稀盐酸制取二氧化碳。
注意:
(1)不能选用稀硫酸,因为稀硫酸与碳酸钙反应生成微溶于水的硫酸钙会橙盖在碳酸钙的表面,阻止反应继续进行。
(2)不能选用浓盐酸,因为浓盐酸易挥发,得不到纯净的二氧化碳气体。
(3)不能用碳酸钠代替石灰石,因为反应太剧烈,产生的气体难以收集。反应速率的快慢与反应物的质量分数和接触面积有关。反应物的接触面积越大,反应物的质量分数越大,反应速率就越快,反之,则越慢。
各组物质反应情况如下表所示:
药品反应速率块状石灰石和稀盐酸产生气泡速率适中石灰石粉末和稀盐酸产生气泡速率很快块状石灰石和稀硫酸产生气泡速率缓慢并逐渐停止碳酸钠粉末和稀盐酸产生气泡速率很快




