题文
根据下列装置图,回答有关问题: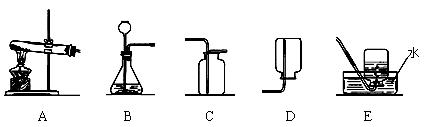
(1)利用上图中A、C装置的组合可以制取某种气体,实验室制取该气体的化学方程式是
,验满方法是 。
(2)实验室通常利用上图中 装置的组合制取二氧化碳(选填字母),该反应的化学方程式为 。
①为了得到纯净、干燥的二氧化碳气体,除杂装置(如右图)的导管按气流方向连接顺序是 (选填字母)。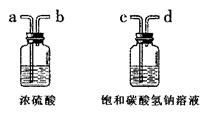
A.a→b→c→d B.b→a→c→d
C.c→d→a→b D.d→c→b→a
②常用澄清石灰水检验二氧化碳的存在,该反应的化学方程式为 ;若二氧化碳过量,二氧化碳又会与碳酸钙、水反应生成易溶的碳酸氢钙[Ca(HCO3)2],该反应的化学方程式为 。向含有氢氧化钙14.8g的石灰水里缓缓通入一定量二氧化碳,充分反应后若生成10g沉淀,则通入二氧化碳的质量可能为 (选填字母)。
A.4.4g B.8.8g C.13.2g D.17.6g
题型:未知 难度:其他题型
答案
(1)2KClO3
2KCl+3O2↑ (或2KMnO4
K2MnO4+MnO2+O2↑)
将带火星的木条靠近集气瓶口,若木条迅速复燃,证明已收集满氧气
(2) BC CaCO3+2HCl===CaCl2+CO2↑+H2O
① C ② CO2+Ca(OH)2===CaCO3↓+ H2O CO2+ CaCO3+ H2O===Ca(HCO3)2 AC
解析
(1)利用上图中A、C装置的组合可以制取氧气,实验室制取该气体的化学方程式是2KClO3
2KCl+3O2↑ (或2KMnO4
K2MnO4+MnO2+O2↑),验满方法是将带火星的木条靠近集气瓶口,若木条迅速复燃,证明已收集满氧气。
(2)实验室制取二氧化碳是固液反应(石灰石和稀盐酸)不要加热的,通常利用上图中BC 装置的组合制取二氧化碳,该反应的化学方程式为CaCO3+2HCl===CaCl2+CO2↑+H2O。
①为了得到纯净、干燥的二氧化碳气体,除杂装置(如右图)的导管按气流方向连接顺序是c→d→a→b;选C。
②常用澄清石灰水检验二氧化碳的存在,该反应的化学方程式为CO2+Ca(OH)2===CaCO3↓+ H2O;若二氧化碳过量,二氧化碳又会与碳酸钙、水反应生成易溶的碳酸氢钙[Ca(HCO3)2],该反应的化学方程式为CO2+ CaCO3+ H2O===Ca(HCO3)2。
向含有氢氧化钙14.8g的石灰水里缓缓通入一定量二氧化碳,充分反应后若生成10g沉淀。
A、若二氧化碳和氢氧化钙恰好反应,则设通入二氧化碳的质量可能为X。
CO2+Ca(OH)2===CaCO3↓+ H2O
44 100
X 10g
44:100=X:10g
X=4.4g
B、若二氧化碳过量,则设二氧化碳质量为Y,碳酸钙质量为Z。
CO2+Ca(OH)2===CaCO3↓+ H2O
44 74 100
Y 14.8g Z
44:74=Y:14.8g
Y=8.8g
74:100=14.8g:Z
Z=20g
即有10g碳酸钙与过量的二氧化碳反应变成了碳酸氢钙。
设与碳酸钙反应的二氧化碳的质量为M。
CO2+ CaCO3+ H2O===Ca(HCO3)2
44 100
M 10g
44:100=M:10g
M=4.4g
此时共通入二氧化碳8.8g+4.4g=13.2g。
选AC。
点评:本题难度较大,特别是最后计算二氧化碳的通入量,要分情况讨论二氧化碳是适量还是过量。验满氧气的方法是将带火星的木条靠近集气瓶口,若木条迅速复燃,证明已收集满氧气。书写化学方程式要遵循客观事实和质量守恒定律两个原则,注意化学式要正确,不要忘记反应条件、气体或者沉淀符号。
考点
据考高分专家说,试题“根据下列装置图,回答有关问题:(1)利用.....”主要考查你对 [氧气的制取和收集 ]考点的理解。
氧气的制取和收集
氧气的制取是初中化学的重点,也是历年中考的热点。我们不仅要学好氧气制取的知识,而且要触类旁通,逐步掌握实验室制取气体的一般思路和方法。中考对制取氧气的考查主要集中在药品选用、实验装置、操作步骤等方面。
实验室制取收集氧气:
过氧化氢制氧气高锰酸钾制氧气药品和反应原理2H2O2
2H2O+O2↑2KMnO4
K2MnO4 + MnO2 + O2↑发生装置固液常温型
固体加热型
收集装置氧气可用排水法收集,也可用向上排空气法收集
整体装置图

操作步骤①检查装置气密性
②再锥形瓶中装入二氧化锰
③塞好带有长颈漏斗和导管的橡皮塞(长颈漏斗的下端一定在液面以下,否则氧气会从长颈漏斗中跑出来)
④向长颈漏斗中加入过氧化氢溶液
⑤收集氧气
①检查装置气密性
②将药品平铺在试管底部,用带导管的单孔橡皮塞塞紧试管口(用高锰酸钾制取氧气,还要在管口放一小团棉花)
③将试管固定在铁架台上
④点燃酒精灯,预热后加热试管
⑤当导管口有连续均匀的气泡冒出时开始收集气体
⑥收集完毕,先将导管移出水面
⑦熄灭酒精灯。加热高锰酸钾(或氯酸钾和二氧化锰的混合物)制氧气,用排水法收集,其操作步骤可概括为:“查”“装”“定”“点”“收”“离”“熄”7个字。可用谐音记忆为“茶庄定点收利息”。 注意事项①伸入试管或锥形瓶中的导管应刚刚露出橡皮塞即可,否则不利于气体的导出。
②用排水法收集氧气时,导管应刚伸人集气瓶口即可,过长不利于水的排出,气体不易收集满。
③用向上排空气法收集氧气时,导管要伸入集气瓶的底部,否则不利于空气的排出,收集的气体不纯。
④用长颈漏斗时,长颈漏斗末端应在液面以下,否则氧气会从长颈漏斗中逸出。 ①药品要平铺在试管底部,均匀受热。
②试管口要略向下倾斜,防止药品中湿存的水分受热后变成水蒸气,遇冷凝结成水倒流回试管底部,使试管炸裂。
③铁架台的铁夹要夹在试管的中上部(或距离试管口1/3处)。
④试管内的导管稍伸出橡皮塞即可,这样便于气体导出。
⑤集气瓶充满水后倒放入水槽中(瓶口要在水面下)。
⑥加热时要先使试管均匀受热,然后酒精灯外焰要对准药品所在部位加热。
⑦用排水法收集气体时,应注意当气泡连续均匀冒出时再收集,否则收集的气体中混有空气,当集气瓶口有大盆气泡冒出时,证明已集满。
⑧停止加热时,应先把导管从水里撤出,再撤掉酒精灯。如果先熄灭酒精灯,试管内气体温度降低,压强减小,水槽中的水就会被倒吸入热的试管内,使试管炸裂。
⑨用高锰酸钾制氧气时,试管口要放一小团棉花,防止加热时高锰酸钾小颗粒进人导管。
⑩盛氧气的集气瓶应盖上玻璃片正放,因为在相同状况下氧气的密度大于空气的密度,正放可减少气体的逸散。




