题文
请结合图回答问题:
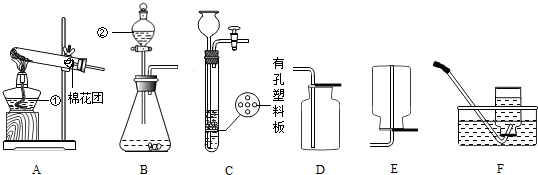
(1)写出图1中有标号仪器的名称:①______;②______.
(2)用加热高锰酸钾的方法制取氧气,应选用的发生装置是______(填字母编号).写出该反应的化学方程式______.
(3)用B,D装置组合可制取某种气体,写出制取该气体的反应化学方程式______.
(4)实验室用锌粒和稀硫酸反应制取氢气,常选用装置B或装置C.C与B相比较其优点是______,选用的收集装置为______(填字母编号)
(5)工业常需要分离H2,CO2的混合气体.某同学采用如图2所示的装置也能达到分离该混合气体的目的.
【操作步骤】
①关闭活塞B,打开活塞A.通入混合气体,可收集到______气体.
②然后,______(填操作),又可收集到另一种气体.
【交流与反思】
通过该分离气体的实验,在选择混合物分离方法时,你得到的启示有______.
题型:未知 难度:其他题型
答案
(1)图中①是酒精灯,②是分液漏斗;
(2)用高锰酸钾制取氧气需要加热反应,所以应选用的发生装置是A;反应方程式是:2KMnO4 △ . K2MnO4+MnO2+O2↑;
(3)B装置适用于固体和液体不需加热制取气体,D装置可收集密度大于空气的气体,所以过氧化氢制取氧气、大理石和稀盐酸反应制取二氧化碳可用B、D装置组合,氢气的密度比空气小,不能用D装置收集,反应方程式分别是:2H2O2 MnO2 . 2H2O+O2↑或CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)C装置中的有空塑料板上放锌粒,反应发生时打开活塞开关,硫酸从长颈漏斗内流下,与锌粒接触反应开始,当关闭开关时气体无法排出,压强越来越大,把硫酸又压回到长颈漏斗内,使锌粒与硫酸分离,所以反应停止,所以该装置可以控制反应的发生和停止;氢气密度小于空气的密度,难溶于水,所以用装置E或F收集;
(5)【操作步骤】①氢气不与氢氧化钠溶液反应,而二氧化碳与氢氧化钠溶液反应,所以关闭活塞B,打开活塞A,通入混合气体,可收集到氢气;
②二氧化碳与氢氧化钠溶液反应生成碳酸钠,碳酸钠与稀硫酸反应生成二氧化碳,所以在完成①之后,关闭活塞A,打开活塞B,这时B中的稀硫酸与步骤①中二氧化碳与氢氧化钠溶液反应生成的碳酸钠反应,生成二氧化碳,所以此时可收集到二氧化碳;
【交流与反思】通过实验可知,在选择混合物分离方法时,可根据气体的性质选取净化剂,且在净化时不减少被净化气体的量,不引进新的杂质,操作简便,易于分离;
故答案为:(1)酒精灯;分液漏斗.
(2)A;2KMnO4 △ . K2MnO4+MnO2+O2↑;
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑或2H2O2 MnO2 . 2H2O+O2↑;
(4)可控制反应的发生和停止;E或F;
(5)【操作步骤】①H2;②关闭活塞A,打开活塞B;
【交流与反思】可根据气体的性质选取净化剂,且在净化时不减少被净化气体的量,不引进新的杂质,操作简便,易于分离(合理均可).
解析
△ .
考点
据考高分专家说,试题“请结合图回答问题:(1)写出图1中有标号.....”主要考查你对 [过滤 ]考点的理解。
过滤
过滤定义:
利用介质滤除水中杂质的方法。
通过特殊装置将流体提纯净化的过程,过滤的方式很多,使用的物系也很广泛,固-液、固-气、大颗粒、小颗粒都很常见。
在推动力或者其他外力作用下悬浮液(或含固体颗粒发热气体)中的液体(或气体)透过介质,固体颗粒及其他物质被过滤介质截留,从而使固体及其他物质与液体(或气体)分离的操作。
过滤归纳:
过滤的原理其中一种能溶于水,另一种不能溶于水,则可以先把它们充分溶于水中,再进行过滤分离制作过滤器把一张圆形滤纸连续对折两次,得到一个四层的扇形滤纸,然后再用手捏住最外面一层滤纸展开,便得到一个一边是一层,另一边是三层的滤纸,用少量水润湿一下,把它贴在漏斗内壁上即可。用到的仪器铁架台(带铁圈)、烧杯、漏斗、玻璃棒、滤纸等过滤装置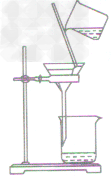
注意事项操作注意事项有:一贴、二低、三靠。
一贴:滤纸紧贴漏斗内壁,以没有气泡为准,可加快过滤的速度;
二低:滤纸边缘低于漏斗边缘;漏斗内液面低于滤纸边缘,防止液体从滤纸与漏斗之间的间隙流下,使过滤不充分;
三靠:盛待过滤液体的烧杯紧靠引流的玻璃棒,防止液体溅到漏斗外丽;玻璃棒的下端紧靠在三层滤纸上,防止戳破滤纸;漏斗下端长的那侧管口紧靠烧杯内壁,防止液体溅出过滤失败的原因①滤纸破损;②过滤时液面高于滤纸边缘; ③收集滤液的烧杯不洁净过滤操作实验口诀斗架烧杯玻璃棒,滤纸漏斗角一样。
过滤之前要静置,三靠两低不要忘。




